题目内容
下列现象或事实可用同一原理解释的是( )
| A、铁分别加入浓硫酸和氢氧化钠溶液中均无明显现象 |
| B、SO2既能使品红褪色也能使酸性高锰酸钾褪色 |
| C、漂白粉溶液和硅酸钠溶液久置空中都变质 |
| D、H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率 |
考点:二氧化硫的化学性质,氯、溴、碘及其化合物的综合应用,铁的化学性质
专题:卤族元素,氧族元素
分析:A.铁与浓硫酸发生钝化反应,与氢氧化钠不反应;
B.二氧化硫具有漂白性,具有还原性;
C.漂白粉与空气中二氧化碳反应生成不稳定的HClO,硅酸钠可生成硅酸;
D.MnO2或FeCl3可催化H2O2的分解.
B.二氧化硫具有漂白性,具有还原性;
C.漂白粉与空气中二氧化碳反应生成不稳定的HClO,硅酸钠可生成硅酸;
D.MnO2或FeCl3可催化H2O2的分解.
解答:
解:A.铁与浓硫酸发生钝化反应,与氢氧化钠不反应,原理不同,故A不选;
B.二氧化硫具有漂白性,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,故B不选;
C.漂白粉与空气中二氧化碳反应生成不稳定的HClO,硅酸钠可生成硅酸,二者原理不同,故C不选;
D.MnO2或FeCl3可催化H2O2的分解,原理相同,故D选.
故选D.
B.二氧化硫具有漂白性,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,故B不选;
C.漂白粉与空气中二氧化碳反应生成不稳定的HClO,硅酸钠可生成硅酸,二者原理不同,故C不选;
D.MnO2或FeCl3可催化H2O2的分解,原理相同,故D选.
故选D.
点评:本题综合考查元素化合物知识,为高考常见题型,注意相关物质的性质,易错点为A,注意铁与浓硫酸发生钝化反应的性质,难度不大.

练习册系列答案
相关题目
下表所列各组物质中,物质之间通过一步反应就能实现如图转化的是( )
| a | b | c |  | |
| A | Al2O3 | AlCl3 | Al(OH)3 | |
| B | CuO | Cu(OH)2 | CuCl2 | |
| C | Si | Na2SiO3 | H2SiO3 | |
| D | CO | NaHCO3 | Na2CO3 |
| A、A | B、B | C、C | D、D |
下列物质中,能使石蕊试液褪色的是( )
| A、二氧化碳 | B、氯气 |
| C、氧化钠 | D、氯化氢 |
常温下a mol?L-1稀氨水和b mol?L-1稀盐酸等体积混合,对混合后溶液判断一定正确的是( )
| A、若a=b,则c(NH4+)=c(Cl-) |
| B、若a>b,则c(NH4+)>c(Cl-) |
| C、若a>b,则c(OH-)>c(H+) |
| D、若a<b,则c(OH-)<c(H+) |
下列图示与对应的叙述相符的是( )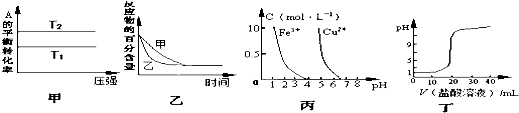

| A、由图甲可以判断:若T1>T2,反应A(g)+B(g)?2C(g)的△H>0 |
| B、图乙表示压强对可逆反应2A(g)+2B(g)?4C(g)+D(s)的影响,乙的压强比甲大 |
| C、根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4 |
| D、图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,pH随加入盐酸体积的变化 |