题目内容
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B、常温常压下24g 金属镁变成Mg2+失去电子2NA |
| C、标准状况下,22.4LH2O含有氢原子个数为2NA |
| D、11.2L氢气一定含有NA 个氢原子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、1mol Na2SO4含1molNa+;
B、根据n=
并结合Mg2+的价态来计算;
C、标况下,水为液态;
D、没指明状态,无法计算氢气的物质的量.
B、根据n=
| m |
| M |
C、标况下,水为液态;
D、没指明状态,无法计算氢气的物质的量.
解答:
解:A、1mol Na2SO4含1molNa+,故溶于水中后所得溶液中Na+个数为2NA,故A错误;
B、24g 金属镁的物质的量n═
=
=1mol,而根据Mg2+的价态可知,1mol金属镁失2mol电子,即2NA个,故B正确;
C、标况下,水为液态,故22.4LH2O的物质的量不是1mol,含有氢原子数不是2NA个,故C错误;
D、没指明状态,不知气体摩尔体积的数值,故无法计算氢气的物质的量,故D错误.
故选B.
B、24g 金属镁的物质的量n═
| m |
| M |
| 24g |
| 24g/mol |
C、标况下,水为液态,故22.4LH2O的物质的量不是1mol,含有氢原子数不是2NA个,故C错误;
D、没指明状态,不知气体摩尔体积的数值,故无法计算氢气的物质的量,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,应在熟练掌握公式使用的基础上,注意物质的组成和机构,难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
能与新制银氨溶液发生“银镜反应”的物质是( )
| A、蛋白质 | B、油脂 |
| C、氨基酸 | D、葡萄糖 |
下列离子方程式正确的是( )
A、碳酸钙中加入盐酸 C
| ||
| B、氢氧化钡与稀硫酸反应 OH-+H+=H2O | ||
C、碳酸钠溶于醋酸溶液 C
| ||
| D、氯化铁溶液与铜反应 Fe3++Cu=Fe2++Cu2+ |
草酸是二元弱酸,草酸氢钾溶液呈酸性.在O.1mol?L-1 KHC2O4溶液中,下列关系正确的是( )
| A、c(HC2O4-)+c(C2O42-)=0.1mol?L-1 |
| B、c(C2O42-)>c(H2C2O4) |
| C、c(K+)=2c(H2C2O4)+2c(HC2O4- )+2c(C2O42-) |
| D、c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O4 2- ) |
质量相同的氧气和二氧化碳中所含原子个数之比为( )
| A、11:8 | B、11:12 |
| C、1:1 | D、3:2 |
在0.lmol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+对于该平衡,下列叙述正确的是( )
| A、加入少量NaOH固体,平衡向正向移动,溶液中c(H+)增大 |
| B、加水,平衡向正向移动,c(CH3COO- )和c(H+)增大 |
| C、通入少量 HCl,平衡逆向移动,溶液中c(H+)减少 |
| D、加入少量CH3COONa固体,平衡向逆向移动,溶液导电能力增强 |
下列物质中,不与盐酸反应,但可与氢氧化钠溶液反应的是( )
| A、Al(OH)3 |
| B、Al2O3 |
| C、SiO2 |
| D、Al |
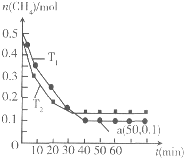 工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )| A、T1>T2 |
| B、b>0 |
| C、K(T1)>K(T2) |
| D、a点时NO2的转化率为33.3% |
下列关于金属保护的说法不正确的是( )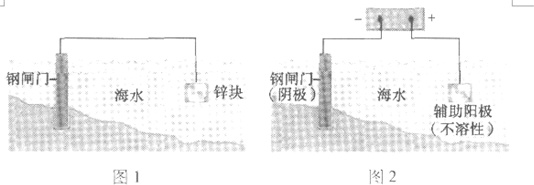

| A、图1是牺牲阳极阴极保护法,图2是外加电流阴极保护法 |
| B、两种保护法共同点是被保护的钢闸门上均为电子流出 |
| C、图1中的负极反应是Zn-2e-═Zn2+ |
| D、图2中钢闸门表面发生还原反应 |