题目内容
16.如图曲线a和b是盐酸与氢氧化钠相互滴定的滴定曲线,下列叙述正确的是( )
| A. | 盐酸的物质的量浓度为1mol/L | |
| B. | P点时恰好完全反应,溶液呈中性 | |
| C. | 曲线a是盐酸滴定氢氧化钠的滴定曲线 | |
| D. | 酚酞不能用作本实验的指示剂 |
分析 根据图知,未加溶液时,a曲线的pH=1,说明该实验是将NaOH滴定稀盐酸,b曲线的pH=13,该实验是将稀盐酸滴定NaOH,
A.未加NaOH溶液时,稀盐酸溶液的pH=1,HCl是强电解质,则c(HCl)=c(H+);
B.P点为a、b曲线相交点,说明这两条曲线的pH相同,此点溶液应该呈中性;
C.根据pH变化曲线知,a是氢氧化钠溶液滴定盐酸溶液,b是盐酸滴定氢氧化钠溶液;
D.氢氧化钠与盐酸恰好反应时溶液呈中性,可用酚酞或甲基橙做指示剂.
解答 解:A.根据图象知,当盐酸中未滴加氢氧化钠溶液时,溶液的pH=1,则c(HCl)=c(H+)=10-1 mol/L=0.1mol/L,故A错误;
B.P点时二者恰好完全中和,盐酸是一元强酸,氢氧化钠是一元强碱,当二者恰好中和时,二者反应生成氯化钠,则溶液呈中性,故B正确;
C.根据图象知,当a曲线发生中和反应时,溶液的pH=1,说明原溶液是盐酸,所以a曲线是氢氧化钠滴定盐酸的实验,故C错误;
D.甲基橙的变色范围是3.1-4.4,酚酞的变色范围是8-10,且变色现象较明显,所以该中和滴定可以用酚酞或甲基橙作指示剂,故D错误;
故选B.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生识图及分析计算能力,正确判断a、b滴定曲线表示的滴定实验是解本题关键,知道指示剂的选取方法,题目难度不大.

练习册系列答案
相关题目
7.在0.1mol•L-1的醋酸溶液中逐渐加入蒸馏水,随着水的加入,在一定时间内始终保增大趋势的是( )
| A. | c(H+) | B. | c(CH3COO-) | ||
| C. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$的比值 | D. | $\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$的比值 |
11.下列说法正确的是( )
| A. | 有机物只能从有机体中取得 | |
| B. | 有机物和无机物的组成、结构、性质有严格区别,它们不能相互转化 | |
| C. | 人类只是从现代才使用有机物 | |
| D. | 合成树脂、合成橡胶、合成纤维等均属于有机物 |
8.某温度下,向一定体积0.1mol•L-1的氨水中逐滴加入等浓度的盐酸,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示.下列说法不正确的是( )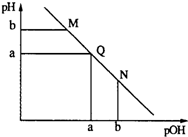

| A. | M点和N点溶液中H2O的电离程度相同 | |
| B. | Q点溶液中,c(NH4+)+c(OH-)=c(Cl-)+c(H+) | |
| C. | M点溶液的导电性大于Q点溶液的导电性 | |
| D. | N点溶液加水稀释,$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$变小 |
5.将相同质量的铜分别与过量浓硝酸、稀硝酸反应,下列叙述正确的是( )
| A. | 消耗硝酸的物质的量:前者少,后者多 | |
| B. | 反应中转移的电子总数:两者相同 | |
| C. | 反应速率:两者相同 | |
| D. | 反应生成气体的颜色:前者浅,后者深 |
6.将I2、Na2O、NaOH、Na2S、Na2SO4分别加热熔化,需要克服相同类型作用力的物质有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
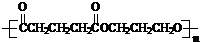 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下: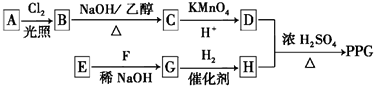
 .
.
 .
. .
. .
.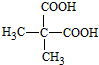 .
. .
.