题目内容
18.下列变化不涉及含硫物质的氧化还原性质的是( )| A. | SO2与H2S气体混合产生S沉淀 | B. | 浓硫酸滴在纸上,纸变黑 | ||
| C. | 二氧化硫在大气中形成酸雨 | D. | 亚硫酸钠在空气中变质 |
分析 S元素的化合价降低,体现氧化性,而S元素的化合价升高体现还原性,以此来解答.
解答 解:A.SO2与H2S气体混合产生S沉淀,S元素的化合价由+4价降低为0,S元素的化合价由-2价升高为0,体现氧化、还原性,故A不选;
B.浓硫酸滴在纸上,纸变黑,与浓硫酸的脱水性有关,与氧化还原无关,故B选;
C.二氧化硫在大气中形成酸雨,亚硫酸被氧化为硫酸,S元素的化合价升高,体现还原性,故C不选;
D.亚硫酸钠在空气中变质,被氧化为硫酸钠,S元素的化合价升高,体现还原性,故D不选;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化、基本概念为解答的关键,侧重分析与应用能力的考查,注意S元素化合价的判断,题目难度不大.

练习册系列答案
相关题目
8.下列化学反应属于吸热反应的是( )
| A. | 生石灰和水的反应 | B. | 木炭在氧气中燃烧 | ||
| C. | 三氧化硫溶于水 | D. | 氢氧化钡晶体与氯化铵晶体混合 |
9.化合物X是一种有机合成中间体,其结构简式如图.下列有关X的说法不正确的是( )
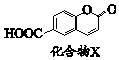
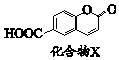
| A. | X分子式是C10H6O4 | |
| B. | X分子中有两种含氧官能团 | |
| C. | 加热条件下1 mol X最多能与2molNaOH反应 | |
| D. | 一定条件下能发生加成、水解、氧化、取代反应 |
6.除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 氢气 | 加热 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 苯(甲苯) | 蒸馏水 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
13.下列有关试剂的保存方法不正确的是( )
| A. | FeSO4溶液中加入Fe粉 | B. | HF保存于玻璃瓶中 | ||
| C. | 铵盐应密封保存于阴凉处 | D. | Na保存于煤油中 |
3.下列实验不合理的是( )
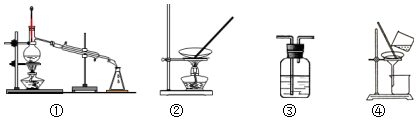

| A. | 用浓硫酸干燥SO2,选③ | |
| B. | 从食盐溶液中获取NaCl,选② | |
| C. | 除去自来水中的Cl-,制纯净水,选④和① | |
| D. | 除去Fe(OH)3胶体中的难溶物,选④ |
10.类推法在学习过程中经常应用.下列左边正确,类推法应用于右边也正确的是( )
| A | 向FeCl2溶液中滴入氯水2Fe2++Cl2=2Fe3++2Cl- | 向FeCl2溶液中滴入碘水2Fe2++I2=2Fe3++2I- |
| B | 用电解熔融NaCl的方法制取金属钠 | 用电解熔融MgCl2的方法制取金属镁 |
| C | pH=3的盐酸稀释1000倍后pH=6 | pH=6的盐酸稀释1000倍后pH=9 |
| D | CO2通入漂白粉溶液中 CO2+Ca2++2ClO-+H2O=CaCO3↓+2HClO | SO2通入漂白粉溶液中 SO2+Ca2++2ClO-+H2O=CaSO3↓+2HClO |
| A. | A | B. | B | C. | C | D. | D |
7.配制某植物营养液可补充氮、磷、钾元素,其成分及含量如表所示:
(1)补充钾元素的物质是K2SO4,其电离方程式为K2SO4═2K++SO42-.
(2)该营养液若在碱性土壤使用,会使氮肥肥效降低,其原因是NH4++OH-═NH3•H2O.
(3)该营养液中磷元素的浓度为3×10-3mol/L.
| 成分 | 含量 (mg/L) |
| 硝酸钙 | 260 |
| 硫酸钾 | 250 |
| 磷酸二氢铵 (NH4H2PO4) M=115g/mol | 345 |
| 硫酸镁 | 537 |
| 硫酸铵 | 237 |
(2)该营养液若在碱性土壤使用,会使氮肥肥效降低,其原因是NH4++OH-═NH3•H2O.
(3)该营养液中磷元素的浓度为3×10-3mol/L.