题目内容
9.将4.3gNa、Na2O、Na2O2的混合物与足量水反应,在标准状况下得到672ml混合气体,将该混合气体通过放电恰好反应,则原混合物中Na、Na2O、Na2O2的物质的量之比为( )| A. | 1:2:1 | B. | 1:1:1 | C. | 1:3:1 | D. | 4:3:2 |
分析 Na、Na2O、Na2O2 的混合物与足量的水反应得到的气体是氢气和氧气的混合物,将该混合气体通过放电,恰好完全反应,说明氢气和氧气反应的物质的量之比恰好等于它们反应的化学计量数之比,氢气来源于钠和水的反应,氧气来源于过氧化钠与水的反应,通过钠与水、过氧化钠与水、氢气和氧气反应的方程式,找出钠与过氧化钠的物质的量之比,据此判断.
解答 解:钠与水、过氧化钠与水、氢气与氧气的反应方程式如下:
2Na+2H2O=2NaOH+H2↑
2Na2O2+2H2O=4NaOH+O2↑
2H2+O2$\frac{\underline{\;放电\;}}{\;}$2H2O
将该混合气体通过放电,恰好完全反应,说明氢气和氧气反应的物质的量之比恰好等于它们反应的计量数之比,即氢气和氧气的物质的量之比为2:1,
由方程式可得钠与过氧化钠的关系式为:4Na~2H2~O2~2Na2O2
所以钠与过氧化钠的物质的量之比为4:2=2:1,而氧化钠的物质的量不确定,
显然D中符合钠与过氧化钠的物质的量之比为2:1,
故选D.
点评 本题考查混合物有关计算,属于无数据计算,难度中等,关键在于氢气与氧气恰好完全反应,再根据方程式中定量比例关系解答.

练习册系列答案
相关题目
19.下列关于元素周期表的说法正确的是( )
| A. | 短周期有一共有3个周期,22种元素 | |
| B. | 元素周期表共有七个周期,十八个族 | |
| C. | 科学研究时,常在周期表金属和非金属的分界线的位置寻找半导体材料 | |
| D. | 元素周期表中每一周期的元素是按照相对原子质量从小到大依次排列 |
20.某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为( )
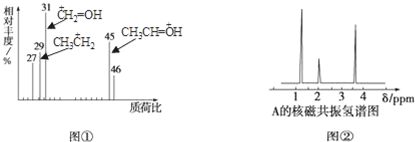

| A. | CH3CH2OH | B. | CH3CHO | C. | CH3OCH3 | D. | CH3CH2COOH |
4.等质量的CuO和MgO粉末分别溶于相同体积的足量硝酸中,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为amol•L-1和bmol•L-1.则a与b的关系为( )
| A. | a=b | B. | a=2b | C. | 2a=b | D. | 无法确定 |
14.下列各组物质间的无色溶液,不用其它试剂即可鉴别的是( )
| A. | NaOH、AlCl3 | B. | H2SO4、BaCl2 | C. | Na2CO3、HCl | D. | AgNO3、KCl |
1.用浓硫酸配制一定物质的量浓度的硫酸溶液,下列操作会造成所配溶液浓度偏高的是( )
| A. | 定容时,眼睛仰视刻度线 | |
| B. | 反复倒转摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好与刻度线相平 | |
| C. | 洗涤烧杯和玻璃棒的溶液未转移入容量瓶中 | |
| D. | 溶解后的溶液未冷却至室温就转移入容量瓶中并定容 |
17.焙烧FeS的反应为 4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2,关于该反应的叙述正确的是( )
| A. | 该反应属于置换反应 | |
| B. | SO2既是氧化产物,又是还原产物 | |
| C. | 每生成1 mol Fe2O3,转移14mol电子 | |
| D. | 若生成2.24LSO2,则生成8g Fe2O3 |
16.下列溶液中的氯离子浓度与50mL 1mol/L的AlCl3溶液中氯离子浓度相等的是( )
| A. | 75 mL 2 mol/L的CaCl2 | B. | 100 mL 2 mol/L的NH4Cl | ||
| C. | 150 mL 1mol/L的KCl | D. | 100 mL 3 mol/L的NaCl |