题目内容
2.K2Cr2O7是一种橙红色具有强氧化性的化合物,当它在酸性条件下被还原成正三价铬时,颜色变为绿色.据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的检验装置吹气.若发现硅胶变色达到一定程度,即可证明司机是酒后驾车.这时酒精被氧化为醋酸其反应原理如下:2K2Cr2O7+3CH3CH2OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O
请结合上面的描述回答下列问题:
(1)将上述反应改写为离子方程式:2Cr2O72-+3CH3CH2OH+16H+=4Cr3++3CH3COOH+11H2O
(2)如果司机属于醉酒驾车,则检验装置中的硅胶将由橙红色变为绿色
(3)上述反应中氧化剂是K2Cr2O7,还原产物是Cr2(SO4)3(本题中的两个空都需填写物质的化学式)
(4)在上述反应中当有69g酒精发生反应时消耗K2Cr2O7的物质的量是1mol.
分析 (1)化学反应中只有乙醇、乙酸、水保留化学式;
(2)酸性条件下被还原成正三价铬时,颜色变为绿色;
(3)Cr元素的化合价降低,得到电子被还原;
(4)结合反应可知,存在2K2Cr2O7~3CH3CH2OH,以此计算.
解答 解:(1)2K2Cr2O7+3CH3CH2OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O中,乙醇、乙酸、水在离子反应中保留化学式,则对应的离子反应为2Cr2O72-+3CH3CH2OH+16H+=4Cr3++3CH3COOH+11H2O,故答案为:2Cr2O72-+3CH3CH2OH+16H+=4Cr3++3CH3COOH+11H2O;
(2)司机属于醉酒驾车,发生2K2Cr2O7+3CH3CH2OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O,还原生成正三价铬时,颜色变为绿色,则观察到装置中的硅胶将由橙红色变为绿色,故答案为:橙红;绿;
(3)Cr元素的化合价降低,则K2Cr2O7为氧化剂,得到电子被还原,Cr2(SO4)3 为还原产物;故答案为:K2Cr2O7;Cr2(SO4)3;
(4)乙醇的物质的量为$\frac{69g}{46g/mol}$=1.5mol,结合反应可知,存在2K2Cr2O7~3CH3CH2OH,则消耗K2Cr2O7的物质的量是1.5mol×$\frac{2}{3}$=1mol,故答案为:1mol.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意计算时存在的物质的量关系,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
12.下列各组中的离子,能在溶液中大量共存的是( )
| A. | K+、NH4+、NO3-、OH- | B. | Ag+、K+、SO42-、Cl- | ||
| C. | H+、Na+、OH-、Cl- | D. | Ca2+、Na+、NO3-、Cl- |
13.反应A(g)+3B(g)?2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速率最大的是( )
| A. | vA=0.15mol•L-1•min-1 | B. | vB=0.6mol•L-1•min-1 | ||
| C. | vC=0.4mol•L-1•min-1 | D. | vD=0.01mol•L-1•s-1 |
10.关于晶体的叙述中,正确的是( )
| A. | 分子晶体中,分子间的作用力越大,该分子越稳定 | |
| B. | 分子晶体中,共价键的键能越大,熔、沸点越高 | |
| C. | 原子晶体中,共价键的键能越大,熔、沸点越高 | |
| D. | 某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
7.相同温度时,甲溶液的PH是5,乙溶液的PH是4.甲、乙两溶液中c(OH-)之比是( )
| A. | 10:1 | B. | 1:10 | C. | 2:1 | D. | 1:2 |
14.下列分子中14个碳原子不可能处在同一平面上的是( )
| A. | 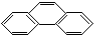 | B. | 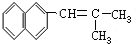 | C. | 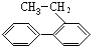 | D. | 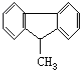 |
11.下列关于物质的类别中,不正确的是(括号内为类别)( )
| A. | H2O(氧化物) | B. | H2SO4(含氧酸) | ||
| C. | CH3COOH(无机物) | D. | I2的CCl4溶液(混合物) |
12.图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )


| A. | 通入 H2电极是负极 | |
| B. | 通入 O2电极发生氧化反应 | |
| C. | 氢氧燃料电池是一种具有应用前景的绿色电源 | |
| D. | 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
 或Na+[:H]-(写一例)
或Na+[:H]-(写一例)