��Ŀ����
6�� ��Ȳ��һ����Ҫ���л��ﻯ��ԭ�ϣ�������Ϊԭ�ϣ��������ת����ϵͼ�����ֲ����Ӧ��������ȥ��������A���ɵ����ʵ�������Ȳ��һ����̼��ˮ��Ӧ���ã�
��Ȳ��һ����Ҫ���л��ﻯ��ԭ�ϣ�������Ϊԭ�ϣ��������ת����ϵͼ�����ֲ����Ӧ��������ȥ��������A���ɵ����ʵ�������Ȳ��һ����̼��ˮ��Ӧ���ã���֪������
 ���ȶ������Զ�ת��R-CH2CHO����ش�
���ȶ������Զ�ת��R-CH2CHO����ش���1��A�����еĹ���������Ϊ̼̼˫�����Ȼ���
��2����Ȳ��F�ķ�Ӧ�����Ǽӳɷ�Ӧ��һ�������£�C��B�ķ�Ӧ������������Ӧ��
��3��E�Ľṹ��ʽΪ
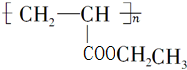 ��
����4������˵������ȷ����BD��ѡ���ţ���
A��F���ڷ��������ұ���ͬϵ�� B��
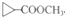 ��D��һ��ͬ���칹��
��D��һ��ͬ���칹��C��D����E�ǵ��壬����E������ D��A��B��D��F�������ʶ���ʹ��ˮ��ɫ
��5��д����ӦA+C��D�Ļ�ѧ����ʽCH2=CHCOOH+CH3CH2OH=CH2=CHCOOCH2CH3+H2O��
���� ��Ȳ��ˮ�ӳ�����B��BΪCH3CHO��CH3CHO����������CΪCH3CH2OH������A��C��Ӧ��������֪���÷�ӦӦΪ������Ӧ��A���ɵ����ʵ�������Ȳ��һ����̼��ˮ��Ӧ���ã���AΪC3H4O2������D��E�ķ���ʽ��֪��D�����Ӿ۷�Ӧ����E�����Կ���֪AΪCH2=CHCOOH������DΪCH2=CHCOOCH2CH3��EΪ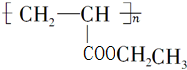 ����Ȳ��ױ������ӳɷ�Ӧ���� F���ݴ˴��⣮
����Ȳ��ױ������ӳɷ�Ӧ���� F���ݴ˴��⣮
��� �⣺��Ȳ��ˮ�ӳ�����B��BΪCH3CHO��CH3CHO����������CΪCH3CH2OH������A��C��Ӧ��������֪���÷�ӦӦΪ������Ӧ��A���ɵ����ʵ�������Ȳ��һ����̼��ˮ��Ӧ���ã���AΪC3H4O2������D��E�ķ���ʽ��֪��D�����Ӿ۷�Ӧ����E�����Կ���֪AΪCH2=CHCOOH������DΪCH2=CHCOOCH2CH3��EΪ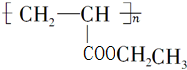 ����Ȳ��ױ������ӳɷ�Ӧ���� F��
����Ȳ��ױ������ӳɷ�Ӧ���� F��
��1��AΪCH2=CHCOOH��A�����еĹ���������Ϊ̼̼˫�����Ȼ���
�ʴ�Ϊ��̼̼˫�����Ȼ���
��2����������ķ�����֪����Ȳ��F�ķ�Ӧ�����Ǽӳɷ�Ӧ��һ�������£�C��B�ķ�Ӧ������������Ӧ��
�ʴ�Ϊ���ӳɷ�Ӧ��������Ӧ��
��3����������ķ�����֪��E�Ľṹ��ʽΪ 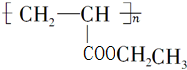 ��
��
�ʴ�Ϊ��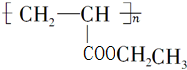 ��
��
��4��A������F�Ľṹ��֪��F���ڷ������������DZ���ͬϵ���A����
B��DΪCH2=CHCOOCH2CH3��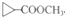 ��D��һ��ͬ���칹�壬��B��ȷ��
��D��һ��ͬ���칹�壬��B��ȷ��
C��D����E�ǵ��壬������E�����ڣ���C����
D��A��B��D��F�������ʺ���ȩ����̼̼˫�������Զ���ʹ��ˮ��ɫ����D��ȷ��
��ѡBD��
��5����ӦA+C��D�Ļ�ѧ����ʽΪCH2=CHCOOH+CH3CH2OH=CH2=CHCOOCH2CH3+H2O��
�ʴ�Ϊ��HCH2=CHCOOH+CH3CH2OH=CH2=CHCOOCH2CH3+H2O��
���� ���⿼���л��ƶϣ��漰ϩ��������ȩ������������Լ�ѧ�����������ȣ��Ƕ��л�������֪ʶ���ۺϿ��飬�ܽϺõĿ��鿼����˼ά������������ϩ��D�ķ���ʽ���ж�D�Ľṹ�ǽ���Ĺؼ����Ѷ��еȣ��Ǹ߿��ȵ����ͣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ���³�ѹ�£�2.8g��ϩ���еĹ��õ��ӶԵ���ĿΪ0.5NA | |
| B�� | ��״���£���11.2LCl2ͨ������������������Һ���Ʊ�Ư��Һ��ת�Ƶĵ�����ΪNA | |
| C�� | VLamol/L���Ȼ�����Һ�У���Fe3+����ĿΪNA����Cl-����Ŀ����3NA | |
| D�� | T��ʱ��1LpH=6�Ĵ�ˮ�У����е�OH-����ĿΪ1.0��10-8NA |
| A�� | �������������ۼ� | B�� | �������������Ӽ� | ||
| C�� | ��������ۼ������Ӽ������� | D�� | ���Ӽ�����������������ۼ� |
| A�� | ʯ�͡�ú����Ȼ������֬�����ڻ�ʯȼ�� | |
| B�� | ��֬�ڼ��������µ�ˮ�ⷴӦ�ֳ�Ϊ������Ӧ | |
| C�� | ����ʽΪ��C6H10O5��n�ĵ��ۺ���ά�ػ�Ϊͬ���칹�� | |
| D�� | �����ǻ�ԭ���ǣ��ܷ���������Ӧ |
| A�� | �������������������Ӧ�����⻯��ķ�����Ϊ�����������������ָ���˷��� | |
| B�� | ��ѧ�ҷ�����������ӫ��ƵIJй�Ч���dz��ã��ɼ��������ķǽ����Ա�һ�����ǿ | |
| C�� | ������������ʶ�ķ�չ�����У����������������۲���������ˮ��Һ���ڷ�ˮ��Һ����ˮ������Ҳ���� | |
| D�� | Ϊ��ʹ��øϴ�·������õ�ϴ��Ч������������ˮ�ܽ�ϴ�·� |
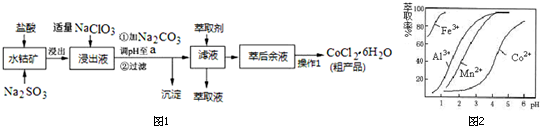
��֪���ٽ���Һ�к��е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Al3+�ȣ�
�ڲ���������������������ʽ����ʱ��Һ��pH���±�������������Ũ��Ϊ��0.01mol/L��
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��1��д������������Co2O3������Ӧ�����ӷ���ʽCo2O3+SO32-+4H+=2Co2++SO42-+2H2O��
��2����������NaClO3�����ǽ�Fe2+����ΪFe3+��Ϊ��߽�ȡ�ʳ����ʵ�����NaClO3Ũ�ȣ������¶Ȼ��ɲ�ȡ��ʩ�ӿ�������ʣ��ʵ��ӳ���ȡʱ�䣻�����ν�ȡ�ȣ�����һ����������������Һ���мӹ���NaClO3ʱ�����ܻ������ж����壬д��ʵ���ҳ������Ʊ�������Ļ�ѧ����ʽMnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��3������Na2CO3��pH��a�����������õ������ֳ����Ļ�ѧʽΪFe��OH��3��Al��OH��3��
��4���Ƶõ�CoCl2•6H2O�ں��ʱ���ѹ��ɵ�ԭ���ǽ��ͺ���¶ȣ���ֹ��Ʒ�ֽ⣮
��5����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ2������Һ���м�����ȡ����Ŀ���dz�ȥ��Һ�е�Mn2+����ʹ�õ����pH��Χ��B��
A��2.0��2.5 B��3.0��3.5 C��4.0��4.5 D��5.0��5.5
��6��Ϊ�ⶨ�ֲ�Ʒ��CoCl2•6H2O��������ȡһ�������Ĵֲ�Ʒ����ˮ����������AgNO3��Һ�����ˡ�ϴ�ӣ���������ɺ����������ͨ�����㷢�ֲִ�Ʒ��CoCl2•6H2O��������������100%����ԭ������Ǵֲ�Ʒ���п������Ȼ������ʧȥ�˲��ֽᾧˮ������һ�����ɣ�
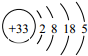 �����й���As����������ȷ���ǣ�������
�����й���As����������ȷ���ǣ�������| A�� | λ�ڵ������ڣ��ڢ�A�� | B�� | ���ڷǽ���Ԫ�� | ||
| C�� | ���ԣ�H3AsO4��H3PO4 | D�� | �ȶ��ԣ�AsH3��PH3 |
| A�� | ����ũ����ո���ȡ�Ҵ� | |
| B�� | ���յع��ͣ��Ʊ�������� | |
| C�� | ���շϾ����ϣ���ֹ��ɫ��Ⱦ | |
| D�� | �������ø�������Դ�����ٶԻ�ʯȼ�ϵ����� |
| A�� | W�ĵ��ʵ��۵���� | |
| B�� | XԪ�صķǽ�������ǿ | |
| C�� | ����������ˮ���ﰴ������ǿ���Լ�����˳����YZWX | |
| D�� | Z��ԭ�Ӱ뾶��� |