题目内容
9.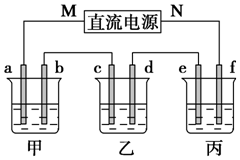 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4的质量分数为10.47%,乙中c电极质量增加.回答问题:
(1)电源的N端为正极;
(2)电极b上发生的电极反应式为4OH--4e-=2H2O+O2↑;
(3)丙装置损失的质量为4.49g(该处保留两位有效数字);电极b上生成的气体在标准状况下的体积为2.8L;
(4)电极c的质量变化是16gg;
(5)①若该直流电源为甲烷燃料电池,电解质溶液为KOH溶液.通入甲烷的铂电极上发生的电极反应式为CH4-8e-+10OH-=CO32-+7H2O.
②已知上述燃料电池中,每转移1mol电子,就有 112KJ的化学能转化为电能.写出常温下甲烷燃烧的热化学方程式CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-896kJ/mol.
分析 (1)该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加,说明c电极是电解池阴极,则d电极是阳极,连接电解池阳极的N端电极是正极;
(2)电解氢氧化钠溶液时,阳极b上氢氧根离子放电生成氧气;
(3)根据丙溶液中水减少的质量结合转移电子数相等计算电极b上生成的气体体积;
(4)根据丙溶液中水减少的质量结合转移电子数相等计算电极c的质量增加;
(5)①燃料电池中,负极上燃料失电子发生氧化反应;
②依据热化学方程式书写热化学方程式,标注物质聚集状态和对应反应的焓变.
解答 解:(1)该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加,说明c电极是电解池阴极,则d电极是阳极,连接电解池阳极的N端电极是正极,故答案为:正;
(2)电解氢氧化钠溶液时,阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑;
(3)l00g 10.00%的K2SO4溶液电解一段时间后K2SO4浓度变为$\frac{100×10%}{10.47%}$,电解硫酸钾溶液实际上是电解的水,所以电解水的质量为100-$\frac{100×10%}{10.47%}$=4.49g,减少4.49g水即为0.25mol.由方程式2H2+O2═2H2O可知,生成2molH2O,转移4mol电子,所以整个反应中转化0.5mol电子,则电极b上生成的气体在标准状况下的体积为$\frac{0.5mol}{4}$×22.4L/mol=2.8L;故答案为:4.49g;2.8L;
(4)因为连接电解池阳极的N端电极是正极,则M为负极,所以c电极为析出铜,由(3)得整个反应中转化0.5mol电子,则电极c增加的质量=$\frac{0.5mol}{2}$×64g/mol=16g.
故答案为:16g;
(5)①甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4-8e-+10OH-=CO32-+7H2O,
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
②每转移1mol电子,就有112KJ的化学能转化为电能,所以1mol甲烷燃烧生成二氧化碳和液态水放热112kJ×8=896kJ,
甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-896kJ/mol;
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-896kJ/mol.
点评 本题考查了原电池原理以及物质的量的有关计算及其热化学方程式的书写,根据转移电子数相等来分析解答即可,难度不大.

| A. | ①②③④ | B. | ②③④ | C. | ③④ | D. | ①② |
| A. | Na2O2 | B. | KOH | C. | CaCl2 | D. | CO2 |
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920℃ | 97.8℃ | 1 291℃ | 190℃ | 2 073℃ | -107℃ | -57℃ | 1 723℃ |
| A. | 只要由金属元素和非金属元素形成的晶体就一定是离子晶体 | |
| B. | 在共价化合物分子中各原子都形成8个电子的稳定结构 | |
| C. | 金属晶体的熔点不一定比分子晶体的高 | |
| D. | 同族元素的氧化物不可能形成不同类型的晶体 |
| A. | 铜和FeCl3溶液均能导电,但二者都不是电解质 | |
| B. | 分解反应的生成物中一定有单质 | |
| C. | 分散质粒子的直径在1×10-9~1×10-7cm之间的分散系属于胶体 | |
| D. | 氯气不能使干燥的有色布条褪色,液氯能使干燥的有色布条褪色 |
| A. | MgO+H2SO4═MgSO4+H2O | B. | Na2O+H2O═2NaOH | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | SO3+H2O═H2SO4 |
| X | Y | ||
| Z | W | Q |
| A. | X、W能与钠形成摩尔质量相同的化合物,且阴阳离子数比为1:2 | |
| B. | X和Z元素形成的化合物广泛应用于制造集成电路、太阳能电池板等 | |
| C. | 氧化物对应的水化物酸性:W<Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |