题目内容
14.用一种试剂除去下列各物质中的杂质(括号内的物质).写出所用试剂及离子方程式.(1)SO42-(CO32-):试剂H2SO4溶液,离子方程式CO32-+2H+=H2O+CO2↑.
(2)Cu粉(Al粉):试剂NaOH溶液或稀硫酸(或稀盐酸),离子方程式2Al+2OH-+2H2O=3H2↑+2AlO2-或2Al+6H+=2Al3++3H2↑.
分析 (1)碳酸根离子与硫酸反应可除杂;
(2)Al与NaOH溶液或硫酸、盐酸反应,而Cu不能,以此来解答.
解答 解:(1)除去碳酸根离子的试剂为H2SO4溶液,发生的离子反应为CO32-+2H+=H2O+CO2↑,故答案为:H2SO4溶液;CO32-+2H+=H2O+CO2↑;
(2)除去Cu粉中的Al粉的试剂为NaOH溶液 或稀硫酸(或稀盐酸),发生的离子反应为2Al+2OH-+2H2O=3H2↑+2AlO2-或 2Al+6H+=2Al3++3H2↑,
故答案为:NaOH溶液 或稀硫酸(或稀盐酸);2Al+2OH-+2H2O=3H2↑+2AlO2-或 2Al+6H+=2Al3++3H2↑.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
4.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 0.1 mol Cl2含有的氯原子数为0.1NA | |
| B. | 3.4 g NH3含有的分子数为0.2NA | |
| C. | 标准状况下,22.4 L H2O含有的分子数为NA | |
| D. | 100 mL 0.1 mol/L的Na2SO4溶液中,Na+数为0.01 NA |
5.下列物质不属于强电解质的是( )
| A. | 硫酸 | B. | 醋酸 | C. | 氢氧化钡 | D. | 硫酸钡 |
2.下列金属不能被稀硫酸腐蚀的是( )
| A. | 黄铜(铜、锌) | B. | 硬铝(铝、铜、镁、硅) | C. | 焊锡(锡、铅) | D. | 18K黄金(金、银、铜) |
19.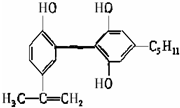 我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )
 我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式为,有关该物质的说法不正确的是( )| A. | 遇FeCl3溶液显紫色 | |
| B. | 1 mol 该物质与浓溴水和H2反应时最多消耗Br2和H2的量分别为4 mol、7 mol | |
| C. | 滴入酸性KMnO4溶液,观察到紫色褪去,可证明结构中存在碳碳双键 | |
| D. | 该分子能和NaOH反应,因为该物质与苯酚一样,都有酚羟基 |
6.下列说法正确的是( )
| A. | FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 | |
| B. | 食盐水中Ca2+、SO42-等杂质的去除,应先加Na2CO3溶液,后加BaCl2溶液 | |
| C. | 用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 | |
| D. | 用BaCl2溶液来检验暴露在空气中的Na2SO3样品是否变质 |
3.下列除去有关物质中杂质的方案中,正确的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质使用的试剂 | 除去杂质的方法 |
| A | Cl2气(HCl气) | NaOH溶液,浓硫酸 | 洗气 |
| B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| C | Na2CO3固体(NaHCO3) | ---- | 灼烧 |
| D | I2 (H2O) | CCl4 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
4.下表中所示实验装置的图示或操作中,不能达到实验目的是( )
| A. | 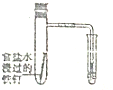 验证铁的析氢腐蚀 | B. | 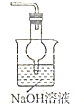 吸收SO2 | ||
| C. | 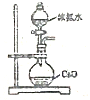 制取少量氨气 | D. | 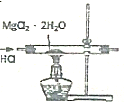 制取无水MgCl2 |