题目内容
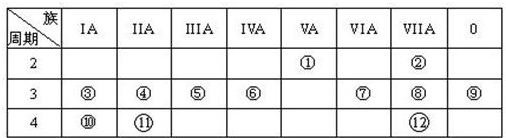
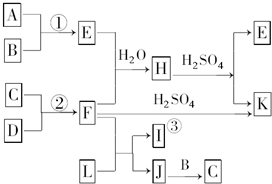
如图是元素周期表的一部分,根据图示回答下列问题:
(1)A、C形成的10电子阳离子的空间构型是 ;写出工业上由GD2合成GD3的化学方程式 ;
(2)E在D2中燃烧生成的化合物X中阴阳离子的个数比为 ;X中的化学键类型是 ;晶体类型是 .
(3)2.00gB2A2完全燃烧生成BD2和液态A2D,放出99.6KJ热量,写出表示B2A2燃烧热的热化学方程式 ;
(4)BD2的电子式为 ;向含E的最高价氧化物的水化物0.05mol的水溶液中通入标况下BD2气体1.12L,其反应离子方程式是 .

(1)A、C形成的10电子阳离子的空间构型是
(2)E在D2中燃烧生成的化合物X中阴阳离子的个数比为
(3)2.00gB2A2完全燃烧生成BD2和液态A2D,放出99.6KJ热量,写出表示B2A2燃烧热的热化学方程式
(4)BD2的电子式为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知A为氢、B为碳、C为氮、D为氧、E为Na、F为Al、G为硫.
(1)A、C形成的10电子阳离子为NH4+;SO2与氧气在催化剂、加热条件下生成SO3;
(2)Na在O2中燃烧生成的化合物X为Na2O2;
(3)计算1molC2H2燃烧放出的热量,标明物质的聚集状态与反应热,书写其燃烧热的热化学方程式;
(4)CO2分子中C原子与氧原子之间形成2对共用电子对;1.12L二氧化碳的物质的量为0.05mol,NaOH为0.05mol,二者按1:1反应恰好生成NaHCO3.
(1)A、C形成的10电子阳离子为NH4+;SO2与氧气在催化剂、加热条件下生成SO3;
(2)Na在O2中燃烧生成的化合物X为Na2O2;
(3)计算1molC2H2燃烧放出的热量,标明物质的聚集状态与反应热,书写其燃烧热的热化学方程式;
(4)CO2分子中C原子与氧原子之间形成2对共用电子对;1.12L二氧化碳的物质的量为0.05mol,NaOH为0.05mol,二者按1:1反应恰好生成NaHCO3.
解答:
解:由元素在周期表中位置,可知A为氢、B为碳、C为氮、D为氧、E为Na、F为Al、G为硫.
(1)A、C形成的10电子阳离子为NH4+,其空间结构为正四面体;SO2与氧气在催化剂、加热条件下生成SO3,反应方程式为:2SO2+O2
2SO3,
故答案为:正四面体;2SO2+O2
2SO3;
(2)Na在O2中燃烧生成的化合物X为Na2O2,过氧化钠中阴阳离子的个数比为1:1,含有化学键类型有:离子键、共价键,属于离子晶体,
故答案为:1:1;离子键、共价键;离子晶体;
(3)1molC2H2燃烧放出的热量=99.6kJ×
=1294.8kJ,C2H2燃烧热的热化学方程式为:C2H2 (g)+
O2(g)═2CO2(g)+H2O(L)△H=-1294.8kJ/mol,
故答案为:C2H2 (g)+
O2(g)═2CO2(g)+H2O(L)△H=-1294.8kJ/mol;
(4)CO2分子中C原子与氧原子之间形成2对共用电子对,电子式为: ;
;
1.12L二氧化碳的物质的量为0.05mol,NaOH为0.05mol,二者按1:1反应恰好生成NaHCO3,离子方程式为:OH-+CO2═HCO3-,
故答案为: ;OH-+CO2═HCO3-.
;OH-+CO2═HCO3-.
(1)A、C形成的10电子阳离子为NH4+,其空间结构为正四面体;SO2与氧气在催化剂、加热条件下生成SO3,反应方程式为:2SO2+O2
| ||
| △ |
故答案为:正四面体;2SO2+O2
| ||
| △ |
(2)Na在O2中燃烧生成的化合物X为Na2O2,过氧化钠中阴阳离子的个数比为1:1,含有化学键类型有:离子键、共价键,属于离子晶体,
故答案为:1:1;离子键、共价键;离子晶体;
(3)1molC2H2燃烧放出的热量=99.6kJ×
| 1mol×26g/mol |
| 2g |
| 5 |
| 2 |
故答案为:C2H2 (g)+
| 5 |
| 2 |
(4)CO2分子中C原子与氧原子之间形成2对共用电子对,电子式为:
 ;
;1.12L二氧化碳的物质的量为0.05mol,NaOH为0.05mol,二者按1:1反应恰好生成NaHCO3,离子方程式为:OH-+CO2═HCO3-,
故答案为:
 ;OH-+CO2═HCO3-.
;OH-+CO2═HCO3-.
点评:本题考查元素周期表、分子结构、晶体类型与化学键、热化学方程式、电子式、离子方程式等,难度不大,(3)中注意燃烧热的热化学方程式中可燃物的系数为1,为易错点.

练习册系列答案
相关题目
对于实验的描述正确的是( )
A、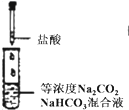 逐滴滴加稀盐酸时,试管中立即产生大量气泡 |
B、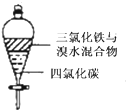 充分振荡后静置,下层溶液为橙红色,上层无色 |
C、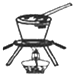 从饱和食盐水中提取NaCl晶体 |
D、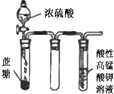 酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |