题目内容
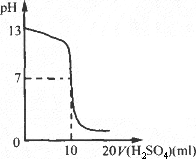
0.05 mol/L H2SO4溶液滴定未知浓度的NaOH溶液,得到的滴定曲线如图所示.
(1)用甲基橙做指示剂,滴定终点时颜色变化是________.
(2)未知浓度NaOH溶液的物质的量浓度是________.
(3)未知浓度NaOH溶液的体积是________.
答案:(1)颜色由红色到橙色;(2)0.1mol/L;(3)10mL
解析:
提示:
解析:
|
本题是利用滴定曲线,讨论酸碱中和的有关问题.这类题目首先要学会看懂题图,深入挖掘题图所蕴含的信息.通过该图我们可以看出,起始碱液的pH为13,由此可求出NaOH溶液的物质的量浓度是0.1 mol/L,硫酸加到10 mL时溶液为中性(pH为7),根据酸碱中和可求出,未知浓度NaOH溶液的体积为10 mL. |
提示:
|
本题是一道图像信息题,在解题时首先要吃透图像蕴含的信息,把这些信息与题目的问题进行有机的结合,可以说,能看懂图像题目就解出了一大半. |

练习册系列答案
相关题目
|
常温下,0.1 mol/L某一元酸(HA)溶液中 | |
| [ ] | |
A. |
溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大 |
B. |
溶液中c(H+)+c(A-)=0.1 mol/L |
C. |
溶液中水电离出的c(H+)=10-10 mol/L |
D. |
与0.05 mol/L NaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A-)>c(Na+)>c(OH-)>c(H+) |