题目内容
把盛有NO2和N2的混合气体的试管倒立在盛水的水槽中,最终液面上升到试管的
处,原混合气体中NO2和N2的体积比是( )
| 1 |
| 3 |
分析:N2和NO2混合气体的试管倒立在水槽中,发生3NO2+H2O═2HNO3+NO,利用体积差来计算混合气体中NO2的体积,以此来解答.
解答:解:设原混合气体中含有xLN2,yLNO2,最终液面上升到距试管底部
处,说明气体体积减小
,N2和NO2 的混合气体的试管倒立于水中发生3NO2+H2O=2HNO3+NO,则
3NO2+H2O=HNO3+NO 体积减小量
3 1 2
y
剩余气体是氮气和一氧化氮,体积为(x+
)L,所以
=
,解得x:y=1:1,
故选A.
| 1 |
| 3 |
| 1 |
| 3 |
3NO2+H2O=HNO3+NO 体积减小量
3 1 2
y
| y |
| 3 |
| 1 |
| 3 |
剩余气体是氮气和一氧化氮,体积为(x+
| y |
| 3 |
| x+y | ||
|
| 3 |
| 2 |
故选A.
点评:本题考查二氧化氮与水的反应及差量法计算,明确发生的化学反应利用差量法计算是解答本题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
把盛有NO2和N2的混合气体的试管倒立在盛水的水槽中,最终液面上升到距试管底部2/3处,则原混合气体中NO2和N2的体积比是
| A.1∶1 | B.1∶2 | C.2∶1 | D.3∶1 |
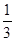 处,原混合气体中NO2和N2的体积比是
处,原混合气体中NO2和N2的体积比是