题目内容
将4 m ol A气体和2 mol B气体在2L 的容器中混合发生如下反应:2A(g)+B(g)
ol A气体和2 mol B气体在2L 的容器中混合发生如下反应:2A(g)+B(g)  2C(g)若经2s 后测得C的浓度为0.6mol•L-1现有下列几种说法其中不正确的是( )
2C(g)若经2s 后测得C的浓度为0.6mol•L-1现有下列几种说法其中不正确的是( )
A. 用物质A表示的反应的平均速率为0.3 mol•L-1•s-1
B. 2s时的压强是起始时的1.1倍
C.  2s时物质A的转化率为30%
2s时物质A的转化率为30%
D. 2s时物质B的浓度为0.7 mol•L-1
现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了测定四种溶液各是什么,将它们随意编号为A、B、C、D后,按下表进行实验。将产生的现象记录如下:
实验顺序 | 实验内容 | 实验现象 |
① | A+B | 没有明显变化 |
② |
| 有无色、无味气体生成 |
③ | B+C | 有白色沉淀生成 |
④ | A+D | 有白色沉淀生成 |
根据实验现象按要求回答:
(1)A、B、C、D溶液中溶质的化学式:
A________;B_________;C________;D________;
(2)写出实验顺序中发生反应的②③④中有关的离子方程式:
②________________;③________________;④_______________。
Ⅰ.在一定条件下,反应A(g)+2B(s) C(g)(正反应为吸热反应)达到平衡后,根据下列图像判断:
C(g)(正反应为吸热反应)达到平衡后,根据下列图像判断:
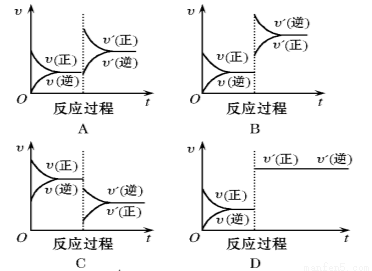
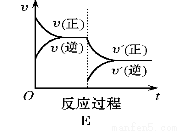
(1)增大压强,达到新平衡的是 (填图像对应的序号,下同)。A的转化率(填“增大”、“减小”、“不变”,下同) 。
(2)增大A的量,达到新平衡的是 ,此时A的转化率 。
Ⅱ.工业合成氨N2(g)+3H2(g) 2NH3(g)反应过程中的能量变化如下图所示,据图回答下列问题:
2NH3(g)反应过程中的能量变化如下图所示,据图回答下列问题:
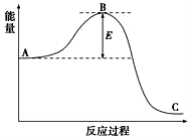
(1)该反应通常用活性铁作催化剂,加活性铁会使图中B点(填“升高”还是“降低”) ,理由是 。
(2)该反应平衡常数表达式为:K= ,增大氮气的量,K (填“增大”、“减小”、“不变”,下同)。
(3)一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的合理措施有 (填字母代号)。
a.高压 b.加入催化剂 c.增加N2的浓度 d.增加H2的浓度 e.分离出NH3
Ⅲ.在一定体积的密闭容器中,进行如下化学反应:其化学平衡常数K与温度t的关系如下:CO2(g)+H2(g)  CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
(1)该反应为 反应。(填“吸热”或“放热”)
(2)830℃,固定容器为2L的密闭容器中,放入混合物,其始浓度为c(CO) =0.1mol/L, c(H2O) =0.3mol/L,经3s后达到平衡,则平衡时CO的物质的量为 ;3s内CO2的平均反应速率为 。
(3)可以判断已知的可逆反应达到平衡状态的是 (填字母代号)。
a.容器内的压强不再变化
b.单位时间内生成amolCO2同时消耗amolCO
c.容器内生成的CO浓度与H2浓度相等
d.单位时间内生成amolCO2同时生成2amolCO
e.单位时间内生成amolCO2同时生成amolH2


 B+D
B+D 上车的是①浓硫酸 ②氰化钾③水银④汽油
上车的是①浓硫酸 ②氰化钾③水银④汽油 精
精 CO(g)+Cl2(g) ΔH>0。
CO(g)+Cl2(g) ΔH>0。 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体 ⑦恒容通入COCl2气体,能提高COCl2转化率的是( )
当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体 ⑦恒容通入COCl2气体,能提高COCl2转化率的是( )