题目内容
用NA表示阿伏加德罗常数,下列叙述中正确的有几项( )
①78gNa2O2与足量的二氧化碳反应,转移电子数目为NA
②足量Fe与标况下22.4L的氯气反应转移电子数目为2NA
③常温常压下16gO2与O3混合气中含有氧原子数目为NA
④0.2mol/LNaOH 溶液中OH+的数目为0.2NA.
①78gNa2O2与足量的二氧化碳反应,转移电子数目为NA
②足量Fe与标况下22.4L的氯气反应转移电子数目为2NA
③常温常压下16gO2与O3混合气中含有氧原子数目为NA
④0.2mol/LNaOH 溶液中OH+的数目为0.2NA.
| A、1项 | B、2项 | C、3项 | D、4项 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:①依据n=
计算物质的量,依据过氧化钠和二氧化碳反应氧元素化合价-1价变化为0价和-2价;
②足量铁和氯气反应生成氯化铁,反应电子转移依据反应的氯气计算;
③依据氧元素守恒计算氧原子数分析;
④溶液体积不知不能计算微粒数;
| m |
| M |
②足量铁和氯气反应生成氯化铁,反应电子转移依据反应的氯气计算;
③依据氧元素守恒计算氧原子数分析;
④溶液体积不知不能计算微粒数;
解答:
解:①依据n=
计算物质的量=
=1mol,过氧化钠和二氧化碳反应氧元素化合价-1价变化为0价和-2价,电子转移为NA,故①正确;
②足量铁和氯气反应生成氯化铁,反应电子转移依据反应的氯气计算,足量Fe与标况下22.4L的氯气反应转移电子数目为2NA,故②正确
③依据氧元素守恒计算氧原子数分析,常温常压下16gO2与O3混合气中含有氧原子数目=
×NA=NA,故③正确;
④溶液体积不知不能计算微粒数,故④错误;
故选C.
| m |
| M |
| 78g |
| 78g/mo |
②足量铁和氯气反应生成氯化铁,反应电子转移依据反应的氯气计算,足量Fe与标况下22.4L的氯气反应转移电子数目为2NA,故②正确
③依据氧元素守恒计算氧原子数分析,常温常压下16gO2与O3混合气中含有氧原子数目=
| 16g |
| 16g/mol |
④溶液体积不知不能计算微粒数,故④错误;
故选C.
点评:本题考查了物质的量计算微粒数,氧化还原反应电子转移计算方法,气体摩尔体积分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
A、 干燥Cl2 |
B、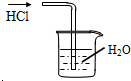 吸收HCl |
C、 石油的蒸馏 |
D、 吸收SO2 |
下列实验一定能证明有SO2存在的是( )
①能使澄清石灰水变浑浊
②能使蓝色石蕊试纸变红色
③能使品红溶液褪色
④通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀生成
⑤先通入足量的NaOH溶液,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸.
①能使澄清石灰水变浑浊
②能使蓝色石蕊试纸变红色
③能使品红溶液褪色
④通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀生成
⑤先通入足量的NaOH溶液,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸.
| A、都能证明 | B、都不能证明 |
| C、③④⑤ | D、④ |
短周期元素的离子aW2+、bX+、cY2、dZ都具有相同的电子层结构,下列推断正确的是( )
| A、原子半径:X>W>Y>Z |
| B、热稳定性:H2Y>HZ |
| C、离子半径:Y2->W2+ |
| D、碱性:W(OH)2>XOH |
有一系列α-氨基酸按如下特点排列:…
该系列化合物中碳元素的质量分数的最大值为( )

该系列化合物中碳元素的质量分数的最大值为( )
| A、85.7% | B、92.3% |
| C、32.0% | D、无法计算 |
NA代表阿伏伽德罗常数的值,下列叙述中正确的是( )
| A、常温下,0.1monCl2与足量NaOH溶液反应,转移的电子数目为0.2NA |
| B、常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
| C、常温常压下,18gH2O2中含有的电子总数为10NA |
| D、标准状况下,22.4L CCl4含有的分子数目为NA |
组成和结构可用 表示的有机物中,苯环两侧能同时发生消去反应的共有( )
表示的有机物中,苯环两侧能同时发生消去反应的共有( )
 表示的有机物中,苯环两侧能同时发生消去反应的共有( )
表示的有机物中,苯环两侧能同时发生消去反应的共有( )| A、8种 | B、10种 |
| C、12种 | D、20种 |
下列说法不正确的是( )
| A、在人类研究物质微观结构的过程中,先后使用了光学显微镜、电子显微镜、扫描隧道显微镜三种不同层次的观测仪器 |
| B、铝硅酸盐分子筛可用于物质分离,还可用作干燥剂、催化剂及催化剂载体 |
| C、使用可再生资源、提高原子经济性、推广利用二氧化碳与环氧丙烷生成的可降解高聚物等都是绿色化学的内容 |
| D、铁盐会水解产生具有吸附性的胶体粒子,可用于饮用水的杀菌消毒 |
 第二周期中碳、氮、氧是构成生命物质的三种主要元素,在生产生活中也有着重要的应用.
第二周期中碳、氮、氧是构成生命物质的三种主要元素,在生产生活中也有着重要的应用.