题目内容
13.X、Y、Z、R、W是原子序数依次增大的五种短周期元素.Y和R同主族,可组成共价化合物,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时0.01mol/LX和W形成 化合物的水溶液pH为2.下列说法不正确的是( )| A. | Y、Z、W三种元素组成化合物的水溶液不一定显碱性 | |
| B. | 在Z、Y形成的两种离子化合物中阴阳离子的个数比分别均为1:2 | |
| C. | 原子半径由大到小排列的顺序是:Z>R>W>Y>X | |
| D. | 由于X、Y组成化合物分之间可以形成氢键,使X、Y组成化合物的稳定性高于X、R组成的化合物 |
分析 X、Y、Z、R、W是原子序数依次增大的五种短周期元素,Y和R同主族,Y处于第二周期,R处于第三周期,可组成共价化合物RY2,则Y为O元素,R为S元素,RY2为SO2;W的原子序数大于硫元素,则W为Cl元素;Y和Z最外层电子数之和与W的最外层电子数相同,则Z的最外层电子数为7-6=1,处于第ⅠA族,原子序数大于氧元素,则Z为Na元素;25℃时0.01mol/L X和W(Cl)形成化合物的水溶液pH为2,则X为H元素,据此进行解答.
解答 解:X、Y、Z、R、W是原子序数依次增大的五种短周期元素,Y和R同主族,Y处于第二周期,R处于第三周期,可组成共价化合物RY2,则Y为O元素,R为S元素,RY2为SO2;W的原子序数大于硫元素,则W为Cl元素;Y和Z最外层电子数之和与W的最外层电子数相同,则Z的最外层电子数为7-6=1,处于第ⅠA族,原子序数大于氧元素,则Z为Na元素;25℃时0.01mol/L X和W(Cl)形成化合物的水溶液pH为2,则X为H元素,
A.Y、Z、W分别为O、Na、Cl,三种元素形成的NaClO3、NaClO4呈中性,故A正确;
B.在Na、O形成的两种离子化台物为Na2O、Na2O2,两种化合物中阴阳离子的个数比分别均为1:2,故B正确;
C.X为H、Y为O、Z为Na、R为S、W为Cl,Na、S、Cl同属于第三周期元素,同周期自左而右原子半径减小,所以Na>S>Cl;H属于第一周期元素,半径最小,O属于第二周期元素,半径大于H小于第三周期元素,则原子半径由大到小排列的是:Z>R>W>Y>X,故C正确;
D.氢化物稳定性与非金属性有关,与氢键无关,由于Y(O)的非金属性大于R(S),则X、Y组成化合物的稳定性高于X、R组成的化合物,故D错误;
故选D.
点评 本题考查位置结构性质关系及应用,题目难度中等,推断元素是解题的关键,“Y、R元素的位置及二者形成的共价化合物RY2”是推断的突破口,注意熟练掌握原子结构与元素周期律、元素周期表的关系.

| A. | Cu | B. | CO2 | C. | NH3 | D. | CH3CH2OH(乙醇) |
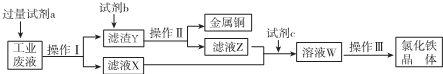
则下列说法正确的是( )
| A. | 试剂a是铁、试剂b是稀硫酸 | |
| B. | 操作I、操作Ⅱ、操作Ⅲ所用仪器相同 | |
| C. | 试剂c可以是H2O2溶液或氯气 | |
| D. | 用酸性KMnO4溶液可检验溶液W中是否还有Fe2+ |
 与足量的氢气和新制备的氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为( )
与足量的氢气和新制备的氢氧化铜反应,消耗的氢气与氢氧化铜的量分别为( )| A. | 1 mol、2 mol | B. | 1 mol、4 mol | C. | 3 mol、2 mol | D. | 3 mol、4 mol |
| A. | 铝是地壳中含量最多的金属元素,在生活中有广泛的应用,但铝制品不宜长时间盛放腌制食品 | |
| B. | 世博停车场安装催化光解设施,可将汽车尾气中的CO和NOX反应生成无毒物质 | |
| C. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| D. | 高容量的储氢材料研究是推广应用氢氧燃料电池的关键问题之一 |
| A. | 向漂白液中通入少量二氧化碳:ClO-+H2O+CO2═${CO}_{3}^{2-}$+2HClO | |
| B. | 常温时偏铝酸钠溶液pH>7:${AlO}_{2}^{-}$+2H2O═Al(OH)3↓+OH- | |
| C. | 等物质的量浓度的FeI2溶液与溴水等体积混合:2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| D. | 向硫酸氢钠溶液中滴加Ba(OH)2溶液恰好至沉淀完全:H++${SO}_{4}^{2-}$+Ba2++OH-═BaSO4↓+H2O |
| A. | 将溶质物质的量之比为2:7的三氯化铝溶液和氢氧化钡溶液混合2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | |
| B. | 将溶质物质的量之比为4:3的 硫酸氢钠和氢氧化钡溶液两溶液混合:4H++3SO42-+3Ba2++4OH-═3BaSO4↓+4H2O | |
| C. | 用石墨电极电解碘化镁溶液 2 I--2 e-=I 2 | |
| D. | 将16.8g 铁粉投入100mL 4.0mol/L的HNO3溶液中(还原产物只有NO)6Fe+20 H++5NO3-═3Fe2++3Fe3++5NO↑+10H2O |
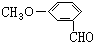 ,有多种同分异构体,其中属于芳香酸的结构简式为:
,有多种同分异构体,其中属于芳香酸的结构简式为: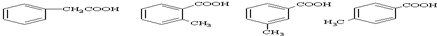 、;
、;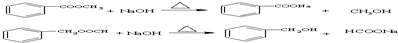 .
.