题目内容
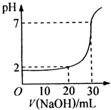 如图为用一定物质的量浓度的NaOH溶液滴定10mL一定物质的量浓度的盐酸的图示.依据图示,推出盐酸和NaOH的物质的量浓度是( )
如图为用一定物质的量浓度的NaOH溶液滴定10mL一定物质的量浓度的盐酸的图示.依据图示,推出盐酸和NaOH的物质的量浓度是( )| 物质的量浓度(mol/L) | A | B | C | D |
| c(HCl) | 0.12 | 0.04 | 0.03 | 0.09 |
| c(NaOH) | 0.04 | 0.12 | 0.09 | 0.03 |
| A、A | B、B | C、C | D、D |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:根据图象知,滴加20mLNaOH溶液时,混合溶液pH=2,滴加30mL溶液时,混合溶液呈中性,说明此时n(HCl)=n(NaOH),HCl和NaOH溶液体积为1:3,则C(HCl)=3C(NaOH),根据20mL混合溶液pH大小确定溶液浓度.
解答:
解:根据图象知,滴加20mLNaOH溶液时,混合溶液pH=2,滴加30mL溶液时,混合溶液呈中性,说明此时n(HCl)=n(NaOH),HCl和NaOH溶液体积为1:3,则C(HCl)=3C(NaOH),
设C(NaOH)为xmol/L,则C(HCl)=3xmol/L,混合溶液pH=2时,
10-2 mol/L=
mol/L,
x=0.03,则C(HCl)=0.09molL,
故选D.
设C(NaOH)为xmol/L,则C(HCl)=3xmol/L,混合溶液pH=2时,
10-2 mol/L=
| 3x×0.01-x×0.02 |
| 0.03 |
x=0.03,则C(HCl)=0.09molL,
故选D.
点评:本题考查混合溶液酸碱性定性判断,侧重考查学生分析问题、计算能力,根据物质之间的反应分析解答即可,注意简单的pH计算方法.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
已知下列热化学方程式:①Zn(s)+
O2(g)═ZnO(s);△H1;②Hg(l)+
O2(g)═HgO(s);△H2.则反应Zn(s)+HgO(s)═Hg(l)+ZnO(s);△H3,△H3为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、△H1-△H2 |
| B、△H2-△H1 |
| C、△H1+△H2 |
| D、-(△H1+△H2) |
对于某些离子的检验及结论一定正确的是( )
| A、加稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| C、加氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| D、加入盐酸没有看到沉淀和气体,说明一定没有发生反应 |
现有四种实验装置,如图所示,要制备硝基苯,应选用( )
A、 |
B、 |
C、 |
D、 |
在4升的密闭容器中,发生以下反应:2A(g)+B(g)?2C(g)+D(g).若最初加入的A和B都是4mol,在前10秒钟A的平均反应速度为0.12mol/(L?s),则10秒钟时,容器中B的物质的量是( )
| A、1.6 mol |
| B、2.8 mol |
| C、2.4 mol |
| D、2.2 mol |
下列有关除杂质(括号中为杂质)的操作中,肯定错误的是( )
| A、乙烷(乙烯):通过盛有足量溴水的洗气瓶 |
| B、溴乙烷(乙醇):多次加水振荡,分液,弃水层 |
| C、苯(甲苯):加酸性高锰酸钾溶液,振荡,分液除去 |
| D、溴苯(溴):加稀氢氧化钠溶液充分振荡洗涤后分液 |
对H2O的电离平衡不产生影响的粒子是( )
A、 |
B、 |
C、 |
| D、26M3+ |