题目内容
化学反应原理的发展在化学的发展史上有重要的推动作用.
(1)用纯净的CaCO3与稀盐酸反应制取CO2气体,请回答:实验过程如图1所示,分析判断 段化学反应速率最快,
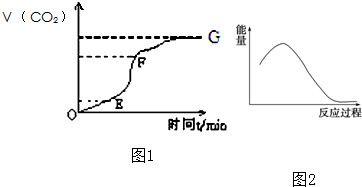
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)下面是一些常见分子的比例模型.其中1个分子中含有共用电子对最多的是
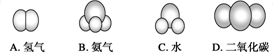
(4)I.20世纪30年代,Eyring和Pzer提出化学反应的过渡态理论:化学反应在反应物到生成物的过程中经过一个高能量的过渡态.如图2是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是 (填“吸热”或“放热”)反应.
Ⅱ.在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:NO2+CO?CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则:
①该段时间内,用CO2表示的平均反应速率为 .
②下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是 (填字母序号).
A.容器内气体的质量保持不变
B.NO2的物质的量浓度不再改变
C.NO2的消耗速率与CO2的消耗速率相等
D.容器内气体的物质的量保持不变.
(1)用纯净的CaCO3与稀盐酸反应制取CO2气体,请回答:实验过程如图1所示,分析判断

(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)下面是一些常见分子的比例模型.其中1个分子中含有共用电子对最多的是
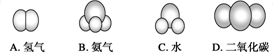
(4)I.20世纪30年代,Eyring和Pzer提出化学反应的过渡态理论:化学反应在反应物到生成物的过程中经过一个高能量的过渡态.如图2是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是
Ⅱ.在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:NO2+CO?CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则:
①该段时间内,用CO2表示的平均反应速率为
②下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.容器内气体的质量保持不变
B.NO2的物质的量浓度不再改变
C.NO2的消耗速率与CO2的消耗速率相等
D.容器内气体的物质的量保持不变.
考点:化学平衡状态的判断,反应热和焓变,化学反应速率的影响因素
专题:基本概念与基本理论
分析:(1)根据曲线斜率判断反应速率;
(2)根据浓度对化学反应速率的影响分析判断;
(3)根据形成共用电子对的数目进行比较;
(4)Ⅰ.根据图中曲线变化判断反应前后能量变化类型;
Ⅱ.①根据反应速率的定义进行计算;
②化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
(2)根据浓度对化学反应速率的影响分析判断;
(3)根据形成共用电子对的数目进行比较;
(4)Ⅰ.根据图中曲线变化判断反应前后能量变化类型;
Ⅱ.①根据反应速率的定义进行计算;
②化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答:
解:(1)曲线斜率大小决定反应速率大小,斜率越大,反应速率越快,所以是EF段;
故答案为:EF;
(2)反应物的浓度越大,反应速率越快,所以只要使反应物浓度变小即可;
A.加蒸馏水,盐酸浓度变小,反应速率减小,故A正确;
B.加氯化钠固体,盐酸浓度不变,反应速率不变,故B错误;
C.加氯化钠溶液,溶液体积增大,盐酸浓度降低,反应速率减小,故C正确;
D.加浓盐酸,盐酸浓度增大,反应速率加快,故D错误;
故答案为:AC
(3)1个氢分子中含有1对共用电子对,1个氨分子中含有3对共用电子对,1个水分子中含有2对共用电子对,1个二氧化碳分子中含有4对共用电子对,
故答案为:D;
(4)I.根据图象可知:反应物的总能量大于生成物的总能量,故该反应是放热反应;
故答案为:放热;
Ⅱ.①NO2+CO?CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则CO2的物质的量为0.2mol,
故v(CO2)=
=
=0.05 mol?(L?min)-1,
故答案为:0.05 mol?(L?min)-1;
②A.容器内的气体反应前后遵循质量守恒,容器内气体的质量保持不变,不一定是平衡状态,故A错误;
B.NO2的物质的量浓度不再改变是平衡状态,故B正确;
C.NO2的消耗速率与CO2的消耗速率相等,说明正逆反应速率相等,是平衡状态,故C正确;
D.反应是一个前后体积不变的反应,容器内气体的物质的量保持不变,不一定是平衡状态,故D错误;
故答案为:BC.
故答案为:EF;
(2)反应物的浓度越大,反应速率越快,所以只要使反应物浓度变小即可;
A.加蒸馏水,盐酸浓度变小,反应速率减小,故A正确;
B.加氯化钠固体,盐酸浓度不变,反应速率不变,故B错误;
C.加氯化钠溶液,溶液体积增大,盐酸浓度降低,反应速率减小,故C正确;
D.加浓盐酸,盐酸浓度增大,反应速率加快,故D错误;
故答案为:AC
(3)1个氢分子中含有1对共用电子对,1个氨分子中含有3对共用电子对,1个水分子中含有2对共用电子对,1个二氧化碳分子中含有4对共用电子对,
故答案为:D;
(4)I.根据图象可知:反应物的总能量大于生成物的总能量,故该反应是放热反应;
故答案为:放热;
Ⅱ.①NO2+CO?CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则CO2的物质的量为0.2mol,
故v(CO2)=
| ||
| t |
| ||
| 2 |
故答案为:0.05 mol?(L?min)-1;
②A.容器内的气体反应前后遵循质量守恒,容器内气体的质量保持不变,不一定是平衡状态,故A错误;
B.NO2的物质的量浓度不再改变是平衡状态,故B正确;
C.NO2的消耗速率与CO2的消耗速率相等,说明正逆反应速率相等,是平衡状态,故C正确;
D.反应是一个前后体积不变的反应,容器内气体的物质的量保持不变,不一定是平衡状态,故D错误;
故答案为:BC.
点评:本题考查反应速率的计算、反应速率和平衡移动的影响因素、共用电子对数目的判断、化学平衡的标志等,综合性较强,难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列离子方程式中,属于水解反应的是( )
| A、CH3COOH+H2O?CH3COO-+H3O+ |
| B、CO2+H2O?HCO3-+H+ |
| C、F-+H2O?HF+OH- |
| D、HS-+H2O?S2-+H3O+ |
下列说法中,正确的是( )
| A、铅笔芯的主要成分是金属铅,儿童在使用是不可用嘴吮吸,以免引起铅中毒 |
| B、CO有毒,在生有炉火的居室中多放几盆水,可吸收CO,防止煤气中毒 |
| C、含氟冰箱产生的氟利昂是造成臭氧空洞的主要原因 |
| D、油条制作中常加入明矾作膨化剂,有利于补充身体所需微量元素,是理想早餐 |
用铂电极电解CuCl2与CuSO4的混合溶液(浓度均为2mol/L)50mL,当阴极析出9.6g固体时,标准状况下阳极得到的气体是( )
| A、2.24L | B、2.8L |
| C、3.36L | D、4.48L |
下列物质的水溶液由于水解而呈碱性的是( )
| A、NaHSO4 |
| B、NaCl |
| C、Na2CO3 |
| D、NH3 |
 2NaIO3+5NaHSO3═3NaHSO4+2Na2SO4+I2+H2O.
2NaIO3+5NaHSO3═3NaHSO4+2Na2SO4+I2+H2O. 实验室需要480mL 0.4mol?L-1的NaCl溶液,有如下操作步骤:
实验室需要480mL 0.4mol?L-1的NaCl溶液,有如下操作步骤: 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图所示:


