题目内容
11.下列各组离子在溶液中一定能大量共存的是( )| A. | Fe3+、NH4+、Cl-、I- | B. | Cu2+、Na+、Cl-、NO3- | ||
| C. | K+、HCO3-、OH-、Ba2+ | D. | K+、CO32-、NO3-、Al3+ |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应、相互促进水解等,则离子大量共存,以此来解答.
解答 解:A.Fe3+、I-发生氧化还原反应,不能共存,故A不选;
B.该组离子之间不反应,可大量共存,故B选;
C.HCO3-、OH-、Ba2+结合生成沉淀和水,不能共存,故C不选;
D.CO32-、Al3+相互促进水解,不能共存,故D不选;
故选B.
点评 本题考查离子共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
9.某学生探究如下实验(A):
(1)使淀粉变蓝的物质是I2.
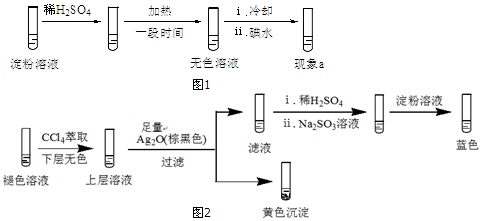
(2)分析现象ⅰ、ⅱ认为:在酸性条件下,加热促进淀粉水解,冷却后平衡逆向移动.设计实验如图1,“现象a”证实该分析不合理:“现象a”是溶液不变蓝.
(3)再次分析:加热后单质碘发生了变化,实验如下:
Ⅰ:取少量碘水,加热至褪色,用淀粉溶液检验挥发出的物质,变蓝.
Ⅱ:向褪色后的溶液中滴加淀粉溶液,冷却过程中一直未变蓝;加入稀H2SO4,瞬间变蓝.
对步骤Ⅱ中稀H2SO4的作用,结合离子方程式,提出一种合理的解释解释1:6H++5I-+IO3-═3I2+3H2O,解释2:4H++4I-+O2═2I2+2H2O,解释3:2H++2I-+IO-═I2+H2O.
(4)探究碘水褪色后溶液的成分:
实验1:测得溶液的pH≈5
实验2:取褪色后的溶液,完成如图2实验:
①产生黄色沉淀的离子方程式是2H++2I-+Ag2O═2AgI↓+H2O.
②Ag2O的作用是证明上层溶液中存在I-,沉淀I-,排除向滤液中加入稀H2SO4后,因I-被氧化生成I2的可能.
③依据上述实验,推测滤液中含有的物质(或离子)可能是HIO(或IO-)、HIO3(或IO3-)、H+.
(5)结合化学反应速率解释实验A中现象ⅰ、现象ⅲ蓝色褪去的原因现象ⅰ:部分I2挥发,部分I2与H2O发生反应;现象ⅲ:淀粉完全水解.加热时,I2与H2O的反应速率大于淀粉水解的速率.
| 实验A | 条件 | 现象 |
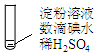 | 加热 | ⅰ.加热后蓝色褪去 ⅱ.冷却过程中,溶液恢复蓝色 ⅲ.一段时间后,蓝色重又褪去 |
(2)分析现象ⅰ、ⅱ认为:在酸性条件下,加热促进淀粉水解,冷却后平衡逆向移动.设计实验如图1,“现象a”证实该分析不合理:“现象a”是溶液不变蓝.
(3)再次分析:加热后单质碘发生了变化,实验如下:
Ⅰ:取少量碘水,加热至褪色,用淀粉溶液检验挥发出的物质,变蓝.
Ⅱ:向褪色后的溶液中滴加淀粉溶液,冷却过程中一直未变蓝;加入稀H2SO4,瞬间变蓝.
对步骤Ⅱ中稀H2SO4的作用,结合离子方程式,提出一种合理的解释解释1:6H++5I-+IO3-═3I2+3H2O,解释2:4H++4I-+O2═2I2+2H2O,解释3:2H++2I-+IO-═I2+H2O.
(4)探究碘水褪色后溶液的成分:
实验1:测得溶液的pH≈5
实验2:取褪色后的溶液,完成如图2实验:
①产生黄色沉淀的离子方程式是2H++2I-+Ag2O═2AgI↓+H2O.
②Ag2O的作用是证明上层溶液中存在I-,沉淀I-,排除向滤液中加入稀H2SO4后,因I-被氧化生成I2的可能.
③依据上述实验,推测滤液中含有的物质(或离子)可能是HIO(或IO-)、HIO3(或IO3-)、H+.
(5)结合化学反应速率解释实验A中现象ⅰ、现象ⅲ蓝色褪去的原因现象ⅰ:部分I2挥发,部分I2与H2O发生反应;现象ⅲ:淀粉完全水解.加热时,I2与H2O的反应速率大于淀粉水解的速率.

6.已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如下表,下列叙述正确的是( )
| 酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡 常数 | Ka=1.75×10-5 | Ka=2.98×10-8 | K1=4.30×10-7 K2=5.61×10-11 | K1=1.54×10-2 K2=1.02×10-7 |
| A. | 将0.1mol/L的醋酸加水不断稀释,c(CH3COO-)始终减小 | |
| B. | 少量CO2通入NaClO溶液中反应的离子方程式为:CO2+H2O+2ClO-=CO32-+2HClO | |
| C. | 少量的SO2通入Ca(ClO)2溶液中反应的离予方程式为:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO | |
| D. | 25℃,等浓度的CH3COOH、HClO、H2CO3和H2SO3溶液中,酸性最强的是HClO |
16. 下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题.
下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题.
(1)非金属性最强的元素是F;
(2)化学性质最不活泼的单质是Ar;
(3)C和O中,原子半径较大的是C;
(4)某原子结构示意图为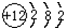 ,其对应的元素符号是Mg;
,其对应的元素符号是Mg;
(5)硫有两种重要氧化物,分别为SO2和SO3(填化学式);
(6)H2S和HCl中,热稳定性较强的是HCl;
(7)NaOH、Mg(OH)2、Al(OH)3中,碱性最强的是NaOH;属于两性氢氧化物的是Al(OH)3;
(8)氮的一种气态氢化物的分子球棍模型如图所示,写出它的化学式NH3,其水溶液显碱性(填“酸性”或“碱性”),此氢化物中N元素和H元素的质量比m(N):m(H)=7:1(相对原子质量:N一14 H-1)
 下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题.
下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题.| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Mg | Al | S | Cl | Ar |
(2)化学性质最不活泼的单质是Ar;
(3)C和O中,原子半径较大的是C;
(4)某原子结构示意图为
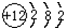 ,其对应的元素符号是Mg;
,其对应的元素符号是Mg;(5)硫有两种重要氧化物,分别为SO2和SO3(填化学式);
(6)H2S和HCl中,热稳定性较强的是HCl;
(7)NaOH、Mg(OH)2、Al(OH)3中,碱性最强的是NaOH;属于两性氢氧化物的是Al(OH)3;
(8)氮的一种气态氢化物的分子球棍模型如图所示,写出它的化学式NH3,其水溶液显碱性(填“酸性”或“碱性”),此氢化物中N元素和H元素的质量比m(N):m(H)=7:1(相对原子质量:N一14 H-1)
20.数据分析能力是新课程对中学生提出的一项要求.表是用沉淀法测定KHCO3和Na2CO3混合物的组成的相关数据.实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液,每次实验均充分反应.实验记录见表:
分析上表数据回答下列问题:
(1)第2次实验中产生沉淀质量是多少克?请将结果填在表格相应空格中.
(2)样品中KHCO3和Na2CO3的物质的量之比是2:3.
(3)室温下,取上述Ba(OH)2溶液50mL,加入0.05mol/L的盐酸,反应后所得溶液的pH=2,求所加盐酸的体积(混合时不考虑溶液体积变化,写出计算过程).
| 实验次数 | 称取样品的质量/g | 所加Ba(OH)2溶液的体积/L | 测得生成沉淀的质量/g |
| 1 | 0.518 | 0.5 | 0.985 |
| 2 | 1.036 | 0.5 | 1.970 |
| 3 | 1.554 | 0.5 | 2.955 |
| 4 | 2.072 | 0.5 | 3.940 |
| 5 | 2.590 | 0.5 | 3.940 |
| 6 | 3.108 | 0.5 | 3.940 |
(1)第2次实验中产生沉淀质量是多少克?请将结果填在表格相应空格中.
(2)样品中KHCO3和Na2CO3的物质的量之比是2:3.
(3)室温下,取上述Ba(OH)2溶液50mL,加入0.05mol/L的盐酸,反应后所得溶液的pH=2,求所加盐酸的体积(混合时不考虑溶液体积变化,写出计算过程).
1.下列关于物质的量的叙述中,错误的是( )
| A. | 1mol任何粒子的粒子数叫做阿伏伽德罗常数 | |
| B. | 1molH2O中含有3mol原子 | |
| C. | 1molH2O中含有2 mol氢和1mol氧 | |
| D. | 0.012Kg12C中约含有6.02×1023个碳原子 |




 .
.