题目内容
某芳香烃A有如下转化关系:

按要求填空:
(1)反应②的反应条件是
(2)写出A和F结构简式:A ;F
(3)写出反应③、⑥对应的化学方程式:③ ;⑥ .

按要求填空:
(1)反应②的反应条件是
(2)写出A和F结构简式:A
(3)写出反应③、⑥对应的化学方程式:③
考点:有机物的合成
专题:有机物的化学性质及推断
分析:D与新制备氢氧化铜反应产物可知A应为 ,则C为
,则C为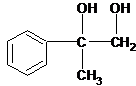 ,B为
,B为 ,则A为
,则A为 ,由最终产物可知F为
,由最终产物可知F为 ,则E为
,则E为 ,据此解答.
,据此解答.
 ,则C为
,则C为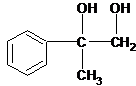 ,B为
,B为 ,则A为
,则A为 ,由最终产物可知F为
,由最终产物可知F为 ,则E为
,则E为 ,据此解答.
,据此解答.解答:
解:D与新制备氢氧化铜反应产物可知A应为 ,则C为
,则C为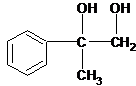 ,B为
,B为 ,则A为
,则A为 ,由最终产物可知F为
,由最终产物可知F为 ,则E为
,则E为 ,
,
(1)反应②为 生成
生成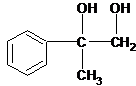 的反应,应在碱性条件下加热发生水解反应生成,故答案为:NaOH溶液、△;
的反应,应在碱性条件下加热发生水解反应生成,故答案为:NaOH溶液、△;
(2)由以上分析可知,A为 ,F为
,F为 ,故答案为:
,故答案为: ;
; ;
;
(3)反应③为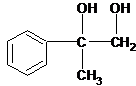 在Cu作催化剂条件下发生氧化反应生成
在Cu作催化剂条件下发生氧化反应生成 的反应,方程式为2
的反应,方程式为2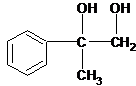 +O2
+O2 2
2  +2H2O,反应⑥对应的化学方程式为:
+2H2O,反应⑥对应的化学方程式为: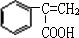 +CH3OH
+CH3OH
 +H2O,
+H2O,
故答案为:2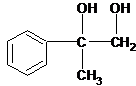 +O2
+O2 2
2  +2H2O;
+2H2O;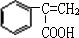 +CH3OH
+CH3OH
 +H2O.
+H2O.
 ,则C为
,则C为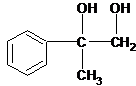 ,B为
,B为 ,则A为
,则A为 ,由最终产物可知F为
,由最终产物可知F为 ,则E为
,则E为 ,
,(1)反应②为
 生成
生成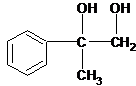 的反应,应在碱性条件下加热发生水解反应生成,故答案为:NaOH溶液、△;
的反应,应在碱性条件下加热发生水解反应生成,故答案为:NaOH溶液、△;(2)由以上分析可知,A为
 ,F为
,F为 ,故答案为:
,故答案为: ;
; ;
;(3)反应③为
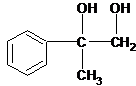 在Cu作催化剂条件下发生氧化反应生成
在Cu作催化剂条件下发生氧化反应生成 的反应,方程式为2
的反应,方程式为2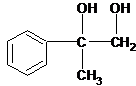 +O2
+O2 2
2  +2H2O,反应⑥对应的化学方程式为:
+2H2O,反应⑥对应的化学方程式为: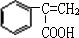 +CH3OH
+CH3OH| 浓硫酸 |
| △ |
 +H2O,
+H2O,故答案为:2
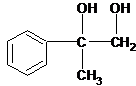 +O2
+O2 2
2  +2H2O;
+2H2O;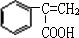 +CH3OH
+CH3OH| 浓硫酸 |
| △ |
 +H2O.
+H2O.
点评:本题考查有机物的推断,题目难度中等,解答本题的关键是以 为突破口进行推断,注意官能团的变化和反应的条件.
为突破口进行推断,注意官能团的变化和反应的条件.
 为突破口进行推断,注意官能团的变化和反应的条件.
为突破口进行推断,注意官能团的变化和反应的条件.
练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ |
| B、草酸使酸性KMnO4溶液褪色:5C2O42-+2MnO4-+16H+═2Mn2++10CO2↑+8H2O |
| C、等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ |
| D、漂白粉溶液中通入少量SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO |
在BaSO4饱和溶液中加入少量BaCl2溶液产生BaSO4沉淀,若以Ksp表示BaSO4的溶度积常数,则平衡后溶液中( )
A、c(Ba2+)=c(SO42-)=
| ||
| B、c(Ba2+)?c(SO42-)>Ksp,c(Ba2+)=c(SO42-) | ||
| C、c(Ba2+)?c(SO42-)=Ksp,c(Ba2+)>c(SO42-) | ||
| D、c(Ba2+)?c(SO42-)≠Ksp,c(Ba2+)<c(SO42-) |
下列各组离子能大量共存,且溶液为无色透明的是( )
| A、K+、S2-、NO3-、H+ |
| B、CrO42-、H+、K+、Cl- |
| C、Ba2+、Na+、HCO3-、OH- |
| D、K+、SO42-、S2-、Na+ |
在溶液中加入适量Na2O2固体后仍能大量共存的离子组是( )
| A、Fe2+、NH4+、Cl-、NO3- |
| B、K+、CO32-、Cl-、SO42- |
| C、Ca2+、Na+、NO3-、HCO3- |
| D、Na+、H+、Cl-、Br- |
在含有0.078mol FeSO4的溶液中通入0.009mol Cl2,再加入含有0.01molX2O72-的溶液后,Fe2+恰好完全转化为Fe3+,则反应后X元素的化合价为( )
| A、+2 | B、+3 | C、+4 | D、+5 |
下列说法错误的是( )
| A、做一次完整的中和热测定实验,温度计至少需使用3次 |
| B、在有盐桥构成的铜(硫酸铜)-锌(硫酸锌)原电池中,盐桥中的阳离子移向电池的锌极 |
| C、利用盖斯定律可间接计算通过实验难测定的反应的反应热 |
| D、可以借助分光光度计采用比色的方法测定某反应的化学反应速率 |
