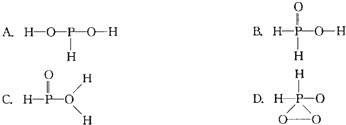题目内容
3.汽车发生强烈碰撞时,安全气囊内的NaN3发生化学反应生成氮化钠(Na3N)与氮气,所产生的气体快速充满气囊,可以达到保护车内人员的目的.(1)请写出上述反应方程式:3NaN3=Na3N+4N2↑;它的基本反应类型是分解反应.
(2)若195g NaN3完全分解,在标准状况下,气囊膨胀的体积约为89.6 L.
(3)28gKOH固体必须溶解在1800g水中,才能使每200个水分子中有1个K+.
分析 1.根据反应物和生成物及其原子守恒书写化学方程式;四种基本反应类型:化合反应、分解反应、置换反应、复分解反应.
2.在化学方程式的计算中,物质的量之比等于系数之比.
3.n=$\frac{m}{M}$=$\frac{N}{NA}$.
解答 (1)根据反应物和生成物及其原子守恒书写化学方程式可得:3NaN3=Na3N+4N2↑;根据反应的形式为“一变多”,故反应属于分解反应;
故答案为:3NaN3=Na3N+4N2↑;分解反应.
(2)195g NaN3完全分解,n( NaN3)=$\frac{195g}{65g•mol-1}$=3mol,由方程式计算可得,n(N2)=4mol,在标况下,V(N2)=4mol×22.4L•mol-1=89.6L
故答案为:89.6 L;
(3)设需要水的质量为xg,由题意可得n(KOH)=$\frac{28g}{56g•mol-1}$=0.5mol,$\frac{0.5NA}{\frac{x•NA}{18}}$=$\frac{1}{200}$,解得x=1800.
故答案为:1800.
点评 本题主要考察了化学方程式的计算,以及化学计量的问题,相对来说比较基础.

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
17.下列4种有机物:
①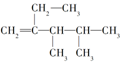
②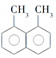
③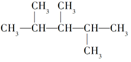
④
其中一氯取代物的同分异构体数目相同的是( )
①

②

③
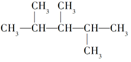
④

其中一氯取代物的同分异构体数目相同的是( )
| A. | ①和② | B. | ②和③ | C. | ①和③ | D. | ②和④ |
18.下列各元素的氧化物中,既能与盐酸反应生成盐和水,又能与NaOH溶液反应生成盐和水的是( )
| A. | 元素X:位于元素周期表中的第三周期ⅢA 族 | |
| B. | 元素Y:它的二价阳离子核外电子总数与氖原子相同 | |
| C. | 元素Z:它的原子中M层比L层少2个电子 | |
| D. | 元素W:它的化合物的焰色反应颜色呈黄色 |
15.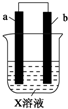 下列对如图所示装置实验现象的描述错误的是( )
下列对如图所示装置实验现象的描述错误的是( )
 下列对如图所示装置实验现象的描述错误的是( )
下列对如图所示装置实验现象的描述错误的是( ) | a电极 | b电极 | X溶液 | |
| ① | Cu | Zn | CuCl2 |
| ② | Zn | 石墨 | HCl |
| A. | 实验①中a极质量增加 | B. | 实验①中Cl-离子向正极移动 | ||
| C. | 实验②a极质量减少 | D. | 实验②中b极放出无色气体 |
2.下列物质间的变化,不能通过与氧气反应一步完成的是( )
| A. | N2→NO2 | B. | Na→Na2O2 | C. | SO2→SO3 | D. | Fe→Fe3O4 |
15.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊;继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊 | Ca(OH)2溶液 |
| B | 通入CO2,溶液变浑浊;继续通CO2至过量,浑浊不消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊;再加入品红溶液,溶液为红色 | Ca(ClO)2溶液 |
| D | 通入SO2,溶液没有明显变化;再通入氨气,溶液变浑浊 | CaCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |
12.NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 1 mol苯分子中含有碳碳双键数为3NA | |
| B. | 常温下,0.1 mol乙烷与乙烯混合气体中所含碳原子数为0.2NA | |
| C. | 14 g乙烯和丙烯的混合气体中所含原子总数为2NA | |
| D. | 标准状况下,22.4 L己烷中共价键数目为19NA |
13.图1是电解饱和氯化钠溶液示意图.图2中,x轴表示实验时流入阴极的电子的物质的量,y轴表示( )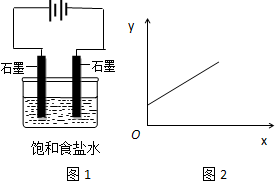

| A. | n(Na+) | B. | n(Cl-) | C. | c(OH-) | D. | c(H+) |
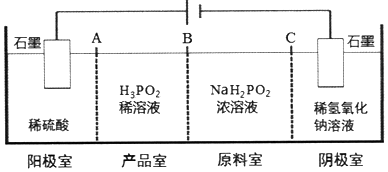
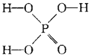 )子中的三个氢原子都可以与重水分子(对D2O)中的D原子发生氢交换.又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)
)子中的三个氢原子都可以与重水分子(对D2O)中的D原子发生氢交换.又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)