题目内容
15.短周期主族元素X、Y、Z、W的原子序数依次递增,四种原子最外层电子数之和为18,X与Z同主族,Y原子的最外层电子数等于周期数,W的单质在常温下为气体.下列说法正确的是( )| A. | 原子半径的大小顺序:r(Z)>r(Y)>r(X) | |
| B. | 简单氢化物的稳定性:W>Z | |
| C. | 元素X的单质只存在两种同素异形体 | |
| D. | X、Y、W最高价氧化物对应的水化物两两之间能发生反应 |
分析 短周期主族元素X、Y、Z、W的原子序数依次递增,Y原子的最外层电子数等于周期数,Y为Al,W的单质在常温下为气体,W为Cl,四种原子最外层电子数之和为18,X与Z同主族,X的最外层电子数为$\frac{18-3-7}{2}$=4,则X为C,Z为Si,以此来解答.
解答 解:由上述分析可知,X为C,Y为Al,Z为Si,W为Cl时,符合题意,
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径的大小顺序为r(Y)>r(Z)>r(X),故A错误;
B.非金属性W>Z,则简单氢化物的稳定性:W>Z,故B正确;
C.碳元素的单质有金刚石、石墨、C60、C70等,故C错误;
D.X、Y、W最高价氧化物对应的水化物分别为碳酸、氢氧化铝、高氯酸,只发生高氯酸与氢氧化铝的反应,故D错误;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、原子结构、元素的位置推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
6. 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )| A. | a 电极发生反应:H2NCH2CH2NH2+16e-+4H2O═2CO2↑+N2↑+16H+ | |
| B. | 质子交换膜处H+由右向左移动 | |
| C. | 该电池在微生物作用下将化学能转化为电能 | |
| D. | 开始放电时b极附近pH不变 |
3.下列物质的性质与应用对应关系正确的是( )
| A. | 氢氟酸具有弱酸性,可用作玻璃蚀刻剂 | |
| B. | 干冰气化时吸热,可用作制冷剂 | |
| C. | 钠与水反应,可用于除去乙醇中少量的水 | |
| D. | 硅酸钠易溶于水,可用作木材防火剂 |
10.某柔性燃料电池(以甲醇为燃料,酸性介质)结构示意如图.下列有关说法正确的是( )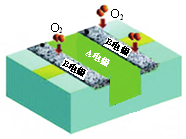

| A. | 电池工作时,电子由A电极经外电路流向B电极 | |
| B. | 电池工作时,减少的化学能完全转化为电能 | |
| C. | A电极发生的电极反应为:CH3OH-6e-+H2O═CO2+6H+ | |
| D. | B电极每消耗1 mol O2,电池中减少4 mol H+ |
20.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结 论 |
| A | 取少量食盐溶于水,加稀硫酸酸化,再滴入淀粉溶液,溶液未呈蓝色 | 该食盐中不含有碘酸钾 |
| B | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,下层溶液显紫红色 | Fe3+的氧化性大于I2 |
| C | 向蛋白质溶液中加入CuCl2或(NH4)2SO4饱和溶液,均有沉淀 | 蛋白质均发生了变性 |
| D | 将0.1mol•L-1,MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液,白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
4.下列有关物质的性质和用途的描述均正确的是( )
| A. | 二氧化锰具有强氧化性.能将双氧水氧化为氧气 | |
| B. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 | |
| C. | 炭具有还原性,可用炭在高温下将二氧化硅还原为硅 | |
| D. | 汽油是常见的有机溶剂,可以用裂化汽油来萃取溴水中的溴 |
16.下列各种物质在一定条件下反应,所得产物种类与反应物的用量或条件无关的是( )
| A. | Ca(HCO3)2溶液与Ca(OH)2反应 | B. | Fe 与 O2反应 | ||
| C. | NaAlO2溶液与CO2反应 | D. | NH4HCO3溶液与NaOH反应 |