题目内容
20.硝酸铵钙晶体[5Ca(NO3)2•NH4NO3•10H2O]极易溶于水,是一种绿色的复合肥料.(1)硝酸铵钙晶体的溶液显酸性,原因是NH4++H2O?NH3•H2O+H+ (用离子方程式表示).
(2)已知磷酸钙是一种难溶物,常温下,其Ksp=2.0×10-33,$\sqrt{2}$≈1.414.工业上生产硝酸铵钙的方法是以硝酸浸取磷矿石得到的粗硝酸钙(含硝酸钙、磷酸钙及硝酸)为原料制备,其生产流程如图1:

①在粗硝酸钙浊液中,c(Ca2+)≈0.1mol/L,则其中c(PO43-)约为1.414×10-15mol/L
②加入适量的碳酸钙后发生反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O.
③硝酸铵是一种易分解的物质,保存和利用时,需控制在较低温度.230~400℃时,它会分解成空气中含量最大的两种气体,其反应的化学方程式为2NH4NO3$\frac{\underline{\;230~400℃\;}}{\;}$2N2↑+O2↑+4H2O.
(3)生产硝酸铵钙工厂的废水中常含有硝酸铵,净化方法有反硝化净化法和电解法.
①NO3-在酸性条件下可转化为N2,该反硝化方法可用半反应(同电极反应式)表示2NO3-+10e-+12H+═6H2O+N2↑.
②目前常用电解法净化,工作原理如图2所示(阳膜和阴膜分别只允许阳离子、阴离子通过);
Ⅰ.阳极的电极反应为2H2O-4e-═4H++O2↑,Ⅰ室可回收的产品为硝酸(填名称).
③Ⅱ.Ⅲ室可回收到氨气,请结合方程式和文字解释其原因电解时Ⅲ室氢离子得电子发生还原反应(或2H++2e-=H2),使碱性增强,同时NH4+通过阳离子膜进入III 室,发生反应:NH4++OH-=NH3+H2O,生成氨气.
分析 (1)铵根离子水解显酸性;
(2)粗硝酸钙(含硝酸钙、难溶物及硝酸)加水溶解,过滤得含硝酸钙和硝酸的溶液,加入碳酸钙与硝酸铵反应生成硝酸铵钙、水和二氧化碳气体,溶液为硝酸钙和硝酸铵的混合溶液,蒸发结晶得到硝酸铵钙[5Ca(NO3)2•NH4NO3•10H2O]晶体.
①根据Ksp[Ca3(PO4)2]=[c(Ca2+)]3×c(PO43-)计算;
②粗硝酸钙(含硝酸钙、难溶物及硝酸)加水溶解,过滤得含硝酸钙和硝酸的溶液,加入碳酸钙与硝酸反应生成硝酸钙、水和二氧化碳气体;
③硝酸铵分解生成氮气和氧气以及水;
(3)①反硝化是利用某些细菌在酸性条件下将NO3-得到电子发生还原反应生成N2,据此书写;
②根据膜电解法阳极上为水失电子发生的氧化反应;Ⅰ室消耗氢氧根离子使酸性增强,与向阳极移动的硝酸根结合成硝酸;
③电解时,Ⅲ室为阴极应为氢离子得电子发生还原反应,消耗氢离子使碱性增强,与向阴极移动的铵根离子反应生成氨气,据此分析.
解答 解:(1)铵根离子水解显酸性,则水解离子反应为NH4++H2O?NH3•H2O+H+,
故答案为:NH4++H2O?NH3•H2O+H+;
(2)①Ksp[Ca3(PO4)2]=2×10-33,c(Ca2+)≈0.1mol/L,Ksp[Ca3(PO4)2]=[c(Ca2+)]3×c(PO43-)=2×10-33,(0.1)3×c2(PO43-)=2×10-33,$\sqrt{2}$≈1.414.c(PO43-)=1.414×10-15mol/L,
故答案为:1.414×10-15mol/L;
②加入碳酸钙与硝酸反应生成硝酸钙、水和二氧化碳气体,发生反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O,
故答案为:CaCO3+2H+═Ca2++CO2↑+H2O;
③空气中含量最大的两种气体分别是氮气和氧气,依据氧化还原反应原理得出硝酸铵分解方程式为:2NH4NO3$\frac{\underline{\;230~400℃\;}}{\;}$2N2↑+O2↑+4H2O,
故答案为:2NH4NO3$\frac{\underline{\;230~400℃\;}}{\;}$2N2↑+O2↑+4H2O;
(3)①反硝化是利用某些细菌在酸性条件下将NO3-转化为N2,即NO3-得到电子发生还原反应生成N2,反应式为2NO3-+10e-+12H+═6H2O+N2↑,
故答案为:2NO3-+10e-+12H+═6H2O+N2↑;
②膜电解法阳极上为水失电子发生的氧化反应,反应式为2H2O-4e-═4H++O2↑,则Ⅰ室阳极消耗氢氧根离子使酸性增强,与向阳极移动的硝酸根结合成硝酸,所以Ⅰ室可回收的产品为硝酸,
故答案为:2H2O-4e-═4H++O2↑;硝酸;
③电解时,Ⅲ室为阴极应为氢离子得电子发生还原反应(或2H++2e-=H2),则消耗氢离子使碱性增强,与向阴极移动的铵根离子反应生成氨气,发生反应:NH4++OH-=NH3+H2O,所以Ⅲ室可回收到氨气,
故答案为:电解时Ⅲ室氢离子得电子发生还原反应(或2H++2e-=H2),使碱性增强,同时NH4+通过阳离子膜进入III 室,发生反应:NH4++OH-=NH3+H2O,生成氨气.
点评 本题主要考查了工业生产硝酸铵钙的原理及废水的处理,意在考查考生阅读新信息,处理新情况的能力,电解装置的分析及其电极反应式的书写是易错点,题目难度中等.

| A. | 用纯净的乙烯合成的聚乙烯是纯净物 | |
| B. | 聚乙烯可以人工合成,也可以是天然高分子化合物 | |
| C. | 聚乙烯高温分解,生成其单体--乙烯 | |
| D. | 聚乙烯的单体能够使溴的四氯化碳溶液褪色 |
| A. | 荔枝酿酒 | B. | 酸雨侵蚀建筑物 | ||
| C. | 空气液化制取氮气 | D. | 生石灰遇水成为碱石灰 |
| A. | c(HCO3-)略大于c(CO32-) | B. | c(HCO3-)等于c(CO32-) | ||
| C. | c(Na+)等于c(CO32-)与c(HCO3-)之和 | D. | c(HCO3-)略小于c(CO32-) |
 2015 年10 月,中国本土科学家屠呦呦因发现青蒿素(见右图)获得诺贝尔生理学或医学奖.青蒿素是继乙氨嘧啶、氯喹、伯喹之后最有效的抗疟特效药,具有速效和低毒的特点,曾被世界卫生组织称做是“世界上唯一有效的疟疾治疗药物”.下列关于青蒿素的说法正确的是( )
2015 年10 月,中国本土科学家屠呦呦因发现青蒿素(见右图)获得诺贝尔生理学或医学奖.青蒿素是继乙氨嘧啶、氯喹、伯喹之后最有效的抗疟特效药,具有速效和低毒的特点,曾被世界卫生组织称做是“世界上唯一有效的疟疾治疗药物”.下列关于青蒿素的说法正确的是( )| A. | 青蒿素的分子式是C15H24O5 | B. | 青蒿素易溶于水 | ||
| C. | 青蒿素能与NaOH 反应 | D. | 青蒿素容易与H2发生加成反应 |
| A. | 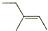 :3-甲基-2-戊烯 :3-甲基-2-戊烯 | B. |  :2-甲基-3-丁炔 :2-甲基-3-丁炔 | ||
| C. | 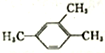 :1,3,4-三甲苯 :1,3,4-三甲苯 | D. | 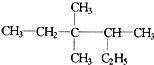 :3,3-二甲基-4-乙基戊烷 :3,3-二甲基-4-乙基戊烷 |
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ•mol-1,则反应物总能量>生成物总能量 | |
| B. | 相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则含1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量 |
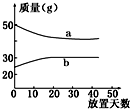 浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )
浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )| A. | a升华、b冷凝 | B. | a蒸发、b吸水 | C. | a蒸发、b潮解 | D. | a冷凝、b吸水 |
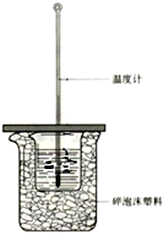 50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图上所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图上所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.