题目内容
2.NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 9g D2O中含有的电子数为5NA | |
| B. | 标准状况下,11.2 L Br2所含的分子数为0.5NA | |
| C. | 7.1g Cl2与足量NaOH溶液反应转移的电子数为0.2NA | |
| D. | 0.1mol CH4所含的电子数为1NA |
分析 A.D2O分子中含有10个电子,20个重水的物质的量为1mol,含有10mol电子;
B.Br2在标准状况下不是气体;
C.71g氯气的物质的量为1mol,氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂;
D.甲烷分子中含有电子数10.
解答 解:A.20个重水的物质的量为1mol,含有10mol电子,9g D2O中含有的电子数小于5NA,故A错误;
B.标准状况下,Br2为液体,11.2 L的Br2物质的量不是0.5mol,故B错误;
C.7.1g Cl2的物质的量为1mol,1mol氯气与足量的NaOH溶液反应转移了1mol电子,转移的电子数为0.1NA,故C错误;
D.0.1mol CH4所含的电子数=0.1mol×10=1NA,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,明确氯气与氢氧化钠溶液的反应中,氯气既是氧化剂又是还原剂.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.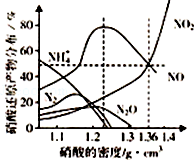 某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )
某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )
 某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )
某些金属与不同密度的硝酸反应时,往往生成多种不同价态的还原产物,如图是在相同条件下,各种不同密度的硝酸和铁反应时,还原产物的分布图.通过图象判断下列说法错误的是( )| A. | 稀硝酸与铁反应,一定有NO生成 | |
| B. | 密度小于1.1g•cm-3的硝酸与铁反应,还原产物百分率最多的是NH4+ | |
| C. | 某硝酸试剂瓶的标签注明:密度为1.26g•cm-3,质量分数50.0%;若取该试剂10ml配成100ml溶液,所得溶液C(H+)=0.1 | |
| D. | 当硝酸的密度为1.36g•cm-3时,过量铁与硝酸反应,消耗的铁与被还原的硝酸物质的量之比为1:1 |
10.两种微粒的质子数相等,电子数也相等,它们不可能是( )
| A. | 一种单质分子和一种化合物分子 | B. | 一种阳离子和一种阴离子 | ||
| C. | 两种不同的阳离子 | D. | 两种不同的阴离子 |
11.合成氨的反应为:3H2+N2?2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol•L-1•s-1),则下列关系正确的是( )
| A. | v(H2)=v(N2)=v(NH3) | B. | v(H2)=3 v(N2) | C. | v(N2)=2 v(NH3) | D. | 2v(NH3)=3v(H2) |