题目内容
3.下列所述事实与化学(离子)方程式相符的是( )| A. | 能说明非金属性Cl>C:2HClO3+CaCO3=Ca(ClO3)2+CO2↑+H2O | |
| B. | 能说明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| C. | 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ | |
| D. | 铅酸蓄电池充电时的负极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
分析 A.比较非金属性强弱应看最高价含氧酸酸性强弱;
B.氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性;
C.氯气足量可以把硫代硫酸钠中的+2价的S都转化为了+6价的S;
D.放电时,该装置是原电池,负极上失电子发生氧化反应.
解答 解:A.氯酸不是最高价含氧酸,所以不能通过2HClO3+CaCO3=Ca(ClO3)2+CO2↑+H2O判断碳与氯元素非金属性强弱,故A错误;
B.2Fe2++H2O2+2H+=2Fe3++2H2O反应中过氧化氢为氧化剂,三价铁离子为氧化产物,所以氧化性H2O2>Fe3+,故B正确;
C.向Na2S2O3溶液中通入足量氯气,离子方程式:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,故C错误;
D.负极上铅失电子和硫酸根离子反应生成硫酸铅,电极反应式为:Pb(s)+SO42-(aq)-2e-=PbSO4(s),故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确物质非金属性强弱判断依据、氧化还原反应强弱规律、原电池工作原理是解题关键,题目难度中等.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
13.高炉炼铁的主要反应为:CO(g)+$\frac{1}{3}$Fe2O3(s)?CO2(g)+$\frac{2}{3}$Fe(s) 已知该反应在不同温度下的平衡常数如下:
下列说法正确的是( )
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
| A. | 增加Fe2O3固体可以提高CO的转化率 | |
| B. | 该反应的△H<0 | |
| C. | 减小容器体积既能提高反应速率又能提高平衡转化率 | |
| D. | 容器内气体密度恒定时,不能标志反应达到平衡状态 |
14.下列说法中正确的是( )
| A. | 在100℃、101 kPa条件下,1 mol液态水汽化时需要吸收40.69 kJ的热量,则H2O(g)═H2O(l)的△H=+40.69 kJ•mol-1 | |||||||||
| B. | 已知CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1,则CH4的燃烧热△H=-890.3 kJ | |||||||||
| C. | H2(g)+Br2(g)═2HBr(g)△H=-72 kJ•mol-1其他相关数据如表:
| |||||||||
| D. | 已知S(g)+O2(g)═SO2(s)△H1,S(g)+O2(g)═SO2(g)△H2,则△H2<△H1 |
11.下列说法正确的是( )
| A. | 结构片段为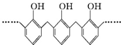 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 | |
| B. | 按系统命名法,有机物(CH3)2CHCH(CH2CH3)CH2CH2CH3命名为:2-甲基-3-乙基庚烷 | |
| C. | 由甘氨酸、丙氨酸形成的二肽有三种 | |
| D. | 乙烯和苯都能使溴水褪色,褪色原理相同 |
18.下列用来解释事实的方程式中不合理的是( )
| A. | 铁丝在氯气中燃烧:Fe+Cl2$\frac{\underline{\;点燃\;}}{\;}$FeCl2 | |
| B. | 常温下,0.1mol/L醋酸溶液pH≈3 CH3COOH?CH3COO-+H+ | |
| C. | 铝片放入氢氧化钠溶液中有气体产生 2Al+2OH-+2H2O=2AlO2-+3H2↑ | |
| D. | 蔗糖与浓硫酸混合产生刺激性气味的气体 C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O |
15.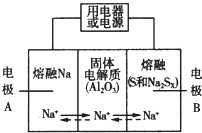 钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
Na2SX$?_{放电}^{充电}$2Na+xS ( 3<x<5 )
(1)根据如表数据,判断该电池工作的适宜温度应为C(选填字母序号).
A.100℃以下
B.100℃~300℃
C.300℃~350℃
D.350℃~2050℃
(2)关于钠硫电池,下列说法正确的是AD(选填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(3)25℃时,若用钠硫电池作为电源电解500mL 0.2mol•L-1NaCl溶液,当溶液的pH变为l3时,电路中通过的电子的物质的量为0.05mol,两极的反应物的质量差为2.3g(假设电解前两极的反应物的质量相等).
 钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$2Na+xS ( 3<x<5 )
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
A.100℃以下
B.100℃~300℃
C.300℃~350℃
D.350℃~2050℃
(2)关于钠硫电池,下列说法正确的是AD(选填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(3)25℃时,若用钠硫电池作为电源电解500mL 0.2mol•L-1NaCl溶液,当溶液的pH变为l3时,电路中通过的电子的物质的量为0.05mol,两极的反应物的质量差为2.3g(假设电解前两极的反应物的质量相等).
13.对于可逆反应A(s)+B(aq)?C(aq)+D(aq)的化学平衡,下列说法正确的是( )
| A. | 温度不变,增大A的物质的量,化学平衡右移 | |
| B. | 温度不变,增大B的浓度,V正增大,V逆减小,化学平衡右移 | |
| C. | 温度不变,减小C的浓度,V逆减小,V正减小,化学平衡右移 | |
| D. | 温度不变,增大D的浓度,同时增大B的浓度,化学平衡一定向左移动 |
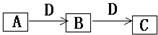 A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化如图所示(部分产物已略去).
A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化如图所示(部分产物已略去).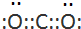 ,及A与C反应的离子方程式:OH-+HCO3-=CO32-+H20;
,及A与C反应的离子方程式:OH-+HCO3-=CO32-+H20;