题目内容
共价键的断裂有均裂和异裂两种方式,即:A:B→A?+B?为均裂;而:A:B→A++[:B]-为异裂.下列化学反应中发生共价键均裂的是( )
| A、2K+2H2O=2KOH+H2↑ |
| B、Na2CO3+Ba(OH)2═BaCO3↓+2NaOH |
| C、SO2+2H2S═2H2O+3S |
| D、Zn+H2SO4═ZnSO4+H2↑ |
考点:共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:根据“A:B→A?+B?为均裂;而:A:B→A++[:B]-为异裂”可知,均裂后形成共价化合物,异裂后产生离子化合物,据此结合各选项中的变化进行解答.
解答:
解:根据题中信息可知:均裂后形成共价化合物,异裂后产生离子化合物,
A.反应2K+2H2O=2KOH+H2↑中,水中共价键形成了离子键,属于共价键异裂,故A错误;
B.Na2CO3+Ba(OH)2═BaCO3↓+2NaOH,反应中没有共价键断裂,故B错误;
C.反应SO2+2H2S═2H2O+3S中,反应物的共价键断裂生成了共价化合物,属于共价键均裂,故C正确;
D.Zn+H2SO4═ZnSO4+H2↑,硫酸中共价键断裂生成离子化合物硫酸锌,属于共价键异裂,故D错误;
故选C.
A.反应2K+2H2O=2KOH+H2↑中,水中共价键形成了离子键,属于共价键异裂,故A错误;
B.Na2CO3+Ba(OH)2═BaCO3↓+2NaOH,反应中没有共价键断裂,故B错误;
C.反应SO2+2H2S═2H2O+3S中,反应物的共价键断裂生成了共价化合物,属于共价键均裂,故C正确;
D.Zn+H2SO4═ZnSO4+H2↑,硫酸中共价键断裂生成离子化合物硫酸锌,属于共价键异裂,故D错误;
故选C.
点评:本题考查以信息的形式考查了共价键的形成及化学键类型,题目难度不大,注意掌握常见化学键的类型,正确理解题干信息为解答本题的关键,试题培养 了学生的分析、理解能力.

练习册系列答案
相关题目
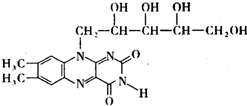 含工业染色剂“苏丹红一号”的有毒食品曾流入市场,引起人们的恐慌.研究表明:核黄素(即维生素B2)能缓解“苏丹红一号”的毒性,其结构如图下列有关核黄素的说法中,正确的是( )
含工业染色剂“苏丹红一号”的有毒食品曾流入市场,引起人们的恐慌.研究表明:核黄素(即维生素B2)能缓解“苏丹红一号”的毒性,其结构如图下列有关核黄素的说法中,正确的是( )| A、核黄素属于分子晶体 |
| B、核黄素能发生银镜反应 |
| C、核黄素属于糖类 |
| D、核黄素不能被酸性高锰酸钾溶液氧化 |
可能含有N2、HCl、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的过氧化钠,气体体积减少;最后通过灼热的铜网,恢复到原来的温度和压强,体积又减少,并有剩余气体.若上述反应均完全,则对混合气体成份的判断正确的是( )
| A、一定有N2和CO2,可能有HCl和CO |
| B、一定有N2,且HCl、CO、CO2中至少含有一种 |
| C、一定有N2、HCl、CO、CO2 |
| D、一定有N2、CO2、CO,一定没有HCl |
能说明甲烷是正四面体形而非正方形平面结构的理由是( )
| A、其一氯取代物不存在同分异构体 |
| B、其二氯取代物不存在同分异构体 |
| C、它有四个C-H共价键 |
| D、它比较稳定,与强酸、强碱不反应 |
秤取160g CuSO4(160g/mol)250g CuSO4?5H2O(250g/mol)分别溶于水时,前者释热66kJ/mol,后者吸热11kJ/mol.则CuSO4(s)+5H2O(l)=CuSO4?5H2O (s) 的热效应是( )
| A、释热77 kJ/mol |
| B、释热55 kJ/mol |
| C、吸热77 kJ/mol |
| D、吸热55 kJ/mol |
有8种物质:①甲烷;②苯;③聚乙烯;④邻二甲苯; ⑤乙炔; 既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A、③④⑤ | B、④⑤ |
| C、只有⑤ | D、全部 |
单质X能从盐溶液中转换出单质Y,由此可知( )
| A、当X、Y都是金属时,X不一定比Y活泼 |
| B、当X、Y都是非金属时,Y一定比X活泼 |
| C、当X是金属时,Y可能是金属也可能是非金属 |
| D、当X是非金属时,Y可能是金属也可能是非金属 |
下列实验操作或装置能达到实验目的是( )
A、 浓硫酸的稀释 |
B、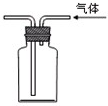 利用排空气法收集CO2 |
C、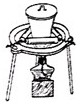 高温灼烧还带成灰 |
D、 制备氨气 |