题目内容
9.向X中持续通入气体Y,不会产生“浑浊→澄清”现象的是( )| A. | X:氯化铝溶液 Y:氨气 | |
| B. | X:氢氧化铁胶体 Y:氯化氢 | |
| C. | X:澄清石灰水 Y:二氧化碳 | |
| D. | X:四羟基合铝酸钠溶液 Y:氯化氢 |
分析 A、氢氧化铝只溶于碱中的强碱,不能溶解在氨水中;
B、氢氧化铁胶体开始遇HCl发生胶体的聚沉;
C、将二氧化碳通入澄清石灰水中后,先生碳酸钙沉淀,后沉淀溶解;
D、四羟基合铝酸钠溶液中通入HCl气体,先生成氢氧化铝沉淀,后沉淀溶解.
解答 解:A、氯化铝溶液中通入氨气,生成的氢氧化铝,不能溶解在氨水中,溶液变浑浊,不会变澄清,故A错误;
B、氢氧化铁胶体开始遇HCl发生胶体的聚沉,生成氢氧化铁沉淀,后继续滴加盐酸,氢氧化铁和盐酸反应生成氯化铁和水而溶解,故B正确;
C、将二氧化碳通入澄清石灰水中后,先生碳酸钙沉淀,当二氧化碳过量时,碳酸钙沉淀和过量的二氧化碳反应生成可溶性的碳酸氢钙,表现为沉淀消失,故C正确;
D、四羟基合铝酸钠溶液中通入HCl气体,开始先生成氢氧化铝沉淀,当HCl过量后,氢氧化铝沉淀溶解,故D正确.
故选A.
点评 本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握发生的氧化还原反应、复分解反应为解答的关键,注意物质的溶解性及氢氧化铝的两性,题目难度不大.

练习册系列答案
相关题目
18.下列四组物质中,互为同位素是( )
| A. | O2和O3 | B. | H216O和H218O | C. | 12C和14C | D. | 正丁烷和异丁烷 |
17.给试管里的固体加热,下列操作中不正确的是( )
| A. | 如试管外壁有水,应在加热前擦拭干净 | |
| B. | 先使试管均匀受热,即先进行预热,然后把灯焰固定在放固体的部位加热 | |
| C. | 试管夹夹在距试管口约$\frac{1}{3}$处 | |
| D. | 加热完毕,立即用冷水冲洗试管 |
4.对于0.1mol•L-1的Na2S溶液,下列判断正确的是( )
| A. | 向溶液中加入少量NaOH固体,能促进水的电离 | |
| B. | c(Na+)=2c(S2-)+c(OH-)+c(HS-) | |
| C. | 向Na2S溶液中加水稀释,其所有离子的浓度都减小 | |
| D. | 溶液中阴离子浓度的大小顺序:c(S2-)>c(OH-)>c(HS-) |
1.相同条件下,相同浓度的盐酸分别与镁、铝、铁3种金属恰好完全反应,产生相同体积的氢气(相同状况下),则下列说法正确的是( )
| A. | 开始时,产生氢气的速率相同 | |
| B. | 参加反应的金属的物质的量比为1:1:1 | |
| C. | 所得溶液的质量相等 | |
| D. | 参加反应的金属的质量比为12:9:28 |
18.下列有关实验的说法正确的是( )
| A. |  图中测定锌粒与1 mol/L稀硫酸反应速率,只需测定量筒中收集氢气的体积 | |
| B. |  装置中进行50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液测定中和热,使温度计温度升高的热量就是中和反应生成1 mol水的热量 | |
| C. |  酸碱中和滴定中,可以在滴定过程中用少量水冲洗锥形瓶内壁以减小实验误差 | |
| D. |  滴定管中读数为26.50mL |
19.氮化铝(AlN)具有耐高温.抗冲击.导热性好等优良性质,被广泛应用于电子工业.陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:
Al2O3+N2+3C$\stackrel{高温}{?}$ 2AlN+3CO下列叙述正确的是( )
Al2O3+N2+3C$\stackrel{高温}{?}$ 2AlN+3CO下列叙述正确的是( )
| A. | 在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂 | |
| B. | 氮化铝是铝合金中的一种 | |
| C. | 上述反应中每生成2molAlN,N失去6mol电子 | |
| D. | 氮化铝中氮元素的化合价为-3 |
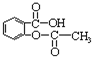 b.烯烃
b.烯烃 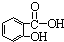 c.炔烃
c.炔烃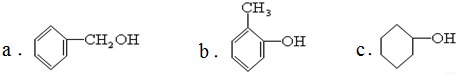
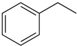 (g)→
(g)→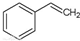 (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol; +CO(g)+H2O(g) △H=+158.8 kJ/mol
+CO(g)+H2O(g) △H=+158.8 kJ/mol