题目内容
(1)在与外界隔离的体系中,自发过程将导致体系的熵 .(填“增大”或“减小”)同一种物质,气态时熵值 (填“最大”或“最小”).
(2)下列物质中:A.NaOH溶液B.Cu C.液态HCl D.液态CH3COOH E.蔗糖溶液 F.液氨 G.氨水 H.硫酸铜晶体 I.石墨 J.无水乙醇
①属于非电解质的是 ;②属于强电解质的是 .
(3)CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ/molCH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.4kJ/mol则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为: .
(2)下列物质中:A.NaOH溶液B.Cu C.液态HCl D.液态CH3COOH E.蔗糖溶液 F.液氨 G.氨水 H.硫酸铜晶体 I.石墨 J.无水乙醇
①属于非电解质的是
(3)CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ/molCH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.4kJ/mol则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:
考点:有关反应热的计算,焓变和熵变,电解质与非电解质,强电解质和弱电解质的概念
专题:
分析:(1)反应能否自发进行取决于焓变和熵变的综合判据,当△G=△H-T?△S<0时,反应可自发进行;对于同一种物质,气态时混乱度最大,即熵值最大;
(2)在水溶液里或熔融状态下都不导电的化合物是非电解质,非电解质首先必须是化合物;强电解质指溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物;
(3)依据热化学方程式和盖斯定律计算得到所需热化学方程式.
(2)在水溶液里或熔融状态下都不导电的化合物是非电解质,非电解质首先必须是化合物;强电解质指溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物;
(3)依据热化学方程式和盖斯定律计算得到所需热化学方程式.
解答:
解:(1)熵是物质微观粒子混乱度(或无序性)的量度,熵值越大,体系内物质微观粒子的混乱度越大,在与外界隔离的体系中,自发过程将导致体系的熵增大,即熵变大于零;对于同一种物质,气态时混乱度最大,即熵值最大,
故答案为:增大;最大;
(2)A.NaOH溶液,能导电,但是混合物,不属于非电解质;
B.Cu能导电,是金属单质,不属于非电解质;
C.液态HCl不能导电,溶于水能完全电离导电,属于强电解质,不属于非电解质;
D.液态CH3COOH不能导电,溶于水部分电离能导电,属于弱电解质,不属于非电解质;
E.蔗糖溶液是混合物,不属于非电解质;
F.液氨属于非电解质;
G.氨水是混合物,不属于电解质和非电解质;
H.硫酸铜晶体,溶于水或熔融状态下能完全电离,能导电,属于强电解质,不属于非电解质;
I.石墨属于非金属单质,不属于电解质和非电解质;
J.无水乙醇,在水溶液里或熔融状态下都不导电,属于非电解质;
所以属于非电解质的是EFJ;属于强电解质的是CH;
故答案为:EFJ;CH;
(3)①CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ?mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.4kJ?mol-1
结合盖斯定律①×2-②得到CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.0kJ/mol,
故答案为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.0kJ/mol.
故答案为:增大;最大;
(2)A.NaOH溶液,能导电,但是混合物,不属于非电解质;
B.Cu能导电,是金属单质,不属于非电解质;
C.液态HCl不能导电,溶于水能完全电离导电,属于强电解质,不属于非电解质;
D.液态CH3COOH不能导电,溶于水部分电离能导电,属于弱电解质,不属于非电解质;
E.蔗糖溶液是混合物,不属于非电解质;
F.液氨属于非电解质;
G.氨水是混合物,不属于电解质和非电解质;
H.硫酸铜晶体,溶于水或熔融状态下能完全电离,能导电,属于强电解质,不属于非电解质;
I.石墨属于非金属单质,不属于电解质和非电解质;
J.无水乙醇,在水溶液里或熔融状态下都不导电,属于非电解质;
所以属于非电解质的是EFJ;属于强电解质的是CH;
故答案为:EFJ;CH;
(3)①CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ?mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.4kJ?mol-1
结合盖斯定律①×2-②得到CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.0kJ/mol,
故答案为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.0kJ/mol.
点评:本题考查了熵变的判断、电解质、非电解质、强电解质等概念的应用、盖斯定律计算和热化学方程式书写方法,题目涉及的知识点较多,掌握基础是关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列分散系能产生丁达尔效应的是( )
| A、硫酸铜溶液 | B、稀硫酸 |
| C、石灰浆 | D、氢氧化铁胶体 |
下列比较不正确的是( )
| A、等浓度的NH4HSO4、NH3?H2O、(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的五种溶液,其中(NH4)2Fe(SO4)2溶液中c(NH4+)最大 |
| B、NaClO和BaCl2混合溶液:c(Na+)+2c(Ba2+)=c(ClO-)+c(HClO)+c(Cl-) |
| C、25℃下,0.2 mol?L-1 HCl溶液与0.2 mol?L-1 YOH(一元弱碱)溶液等体积混合(忽略混合后溶液体积的变化),则c(Cl-)=c(Y+)+c(YOH)=0.2 mol?L-1 |
| D、常温下,将0.2 mol?L-1某一元碱ROH溶液和0.1 mol?L-1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+) |
进行实验必须注意安全,下列说法正确的是( )
| A、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B、不慎将浓碱溶液沾到皮肤上,要立即用盐酸冲洗 |
| C、用点燃的火柴在液化气钢瓶口检验是否漏气 |
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
下列电池工作时,O2在正极放电的是( )
 |  |  |  |
| A.锌锰电池 | B.氨燃料电池 | C.铅蓄电池 | D.镍镉电池 |
| A、A | B、B | C、C | D、D |
下列分子,各原子均处于同一平面上的是( )
| A、NH3 |
| B、CCl4 |
| C、C2H4 |
| D、PCl3 |
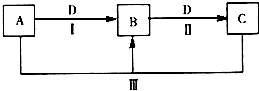 A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化关系如图所示(部分产物已略去).
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化关系如图所示(部分产物已略去).