题目内容
(1)镍是银白色金属,在常温下对水和空气都较稳定,能抗碱性腐蚀,故实验室中可以用镍坩埚熔融碱.Ni2+的核外电子排布式为 .
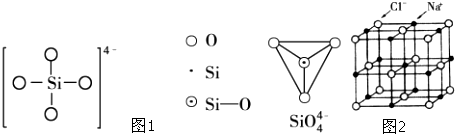
(2)已知原硅酸根离子SiO44-为四面体结构,该离子的结构式和空间结构图1可表示为:二聚硅酸根离子Si2O76-中,只有硅氧键,则它的结构式和空间结构图可表示为 , .
(3)煤液化获得甲醇,再经催化氧化可得到重要工业原料甲醛,甲醇的沸点比甲醛的高,其主要原因是 ;甲醛分子中碳原子轨道的杂化类型为 ;1mol甲醛分子中键的数目为 .煤炭液化所用的一种催化剂含有铜元素,如下表所示铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是 .
(4)图2是氯化钠晶胞的结构示意图,其中与每个Na+距离最近且等距离的几个Cl-所围成的空间的构型为 ,该品胞沿体对角线方向投影的几何形状为 ,该投影图中Na+和Cl-的比例为 (被遮挡的原子不计人在内.)
(2)已知原硅酸根离子SiO44-为四面体结构,该离子的结构式和空间结构图1可表示为:二聚硅酸根离子Si2O76-中,只有硅氧键,则它的结构式和空间结构图可表示为

(3)煤液化获得甲醇,再经催化氧化可得到重要工业原料甲醛,甲醇的沸点比甲醛的高,其主要原因是
| 电离能/kJ?mol-1 | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
考点:判断简单分子或离子的构型,原子核外电子排布,元素电离能、电负性的含义及应用,晶胞的计算,原子轨道杂化方式及杂化类型判断
专题:原子组成与结构专题,化学键与晶体结构
分析:(1)镍原子核外电子数是28,镍原子失去最外层2个电子变成基态Ni2+,根据构造原理书写基态Ni2+的核外电子排布式;
(2)根据每个四面体中心含有1个Si原子,每个硅原子周围结合4个氧原子,同时每个氧原子跟2个硅原子结合,因此二氧化硅晶体(石英)是由氧、硅原子按原子个数1:2组成的立体空间网状结构的原子晶体,Si2O76-只有硅氧键,据此书写结构式和空间结构图;
(3)甲醇存在氢键,沸点较高,甲醛(HCHO)中C原子形成3个σ键,以此判断杂化类型;轨道中电子处于全满、全空、半满时较稳定;
(4)将与Cl-距离最近Na+连接后判断;沿体对角线方向投影的几何形状为正六边形;该投影图中Na+和Cl-的比例为9:10;
(2)根据每个四面体中心含有1个Si原子,每个硅原子周围结合4个氧原子,同时每个氧原子跟2个硅原子结合,因此二氧化硅晶体(石英)是由氧、硅原子按原子个数1:2组成的立体空间网状结构的原子晶体,Si2O76-只有硅氧键,据此书写结构式和空间结构图;
(3)甲醇存在氢键,沸点较高,甲醛(HCHO)中C原子形成3个σ键,以此判断杂化类型;轨道中电子处于全满、全空、半满时较稳定;
(4)将与Cl-距离最近Na+连接后判断;沿体对角线方向投影的几何形状为正六边形;该投影图中Na+和Cl-的比例为9:10;
解答:
解:(1)镍原子核外电子数是28,镍原子失去最外层2个电子变成基态Ni2+,根据构造原理知,基态Ni2+的核外电子排布式为1s22s22p63s23p63d8(或[Ar]3d8),
故答案为:1s22s22p63s23p63d8(或[Ar]3d8);
(2)原硅酸(H4SiO4)的结构可表示为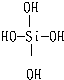 ,两个原硅酸分子可发生分子间脱水生成二聚原硅酸
,两个原硅酸分子可发生分子间脱水生成二聚原硅酸 :二聚原硅酸电离出6个H+后,形成带6个负电荷的二聚原硅酸根离子,以此二聚硅酸根离子的结构可表示为:
:二聚原硅酸电离出6个H+后,形成带6个负电荷的二聚原硅酸根离子,以此二聚硅酸根离子的结构可表示为: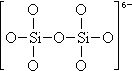 ,每个四面体中心含有1个Si原子,硅原子位居该四面体中心,四个氧原子各占一个顶点,为无支链的单环状,Si2O76-只有硅氧键,通过共用氧原子的形式构成,所以它的空间结构图可表示为:
,每个四面体中心含有1个Si原子,硅原子位居该四面体中心,四个氧原子各占一个顶点,为无支链的单环状,Si2O76-只有硅氧键,通过共用氧原子的形式构成,所以它的空间结构图可表示为: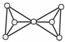 ,
,
故答案为: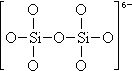 ;
; ;
;
(3)甲醇分子之间形成氢键,沸点较高,甲醛(HCHO)中C原子形成3个σ键,碳原子轨道的杂化类型为sp2杂化,1mol甲醛分子中σ键的数目为3NA;轨道中电子处于全满、全空、半满时较稳定,所以气态Cu失去一个电子变成结构为[Ar]3d10的Cu+,能量较低,所以Cu的第二电离能相对较大(或气态Zn失去一个电子变成结构为[Ar]3d104s1的Zn+,易再失去一个电子,所以Zn的第二电离能相对较小),
故答案为:甲醇分子之间形成氢键;sp2杂化;3NA;Cu失去一个电子变成结构为[Ar]3d10的Cu+,属于能量较低稳定结构,所以Cu的第二电离能相对较大(或气态Zn失去一个电子变成结构为[Ar]3d104s1的Zn+,易再失去一个电子,所以Zn的第二电离能相对较小);
(4)沿X、Y、Z三轴切割的方法知,X轴上有2个氯离子,Y轴上有2个氯离子,Z轴上有2个氯离子,所以钠离子的配位数是6,将6个氯离子连接后所围成的空间几何构型正八面体,沿体对角线方向投影的几何形状为正六边形,晶体中每个Cl-同时吸引着6个Na+,每个钠离子同时吸引着6个氯离子,晶体中在每个Cl-周围与它最接近且距离相等的Cl-个数=3×8×
=12,所以该投影图中Na+和Cl-的比例为9:10;
故答案为:正八面体;正六边形;9:10;
故答案为:1s22s22p63s23p63d8(或[Ar]3d8);
(2)原硅酸(H4SiO4)的结构可表示为
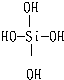 ,两个原硅酸分子可发生分子间脱水生成二聚原硅酸
,两个原硅酸分子可发生分子间脱水生成二聚原硅酸 :二聚原硅酸电离出6个H+后,形成带6个负电荷的二聚原硅酸根离子,以此二聚硅酸根离子的结构可表示为:
:二聚原硅酸电离出6个H+后,形成带6个负电荷的二聚原硅酸根离子,以此二聚硅酸根离子的结构可表示为: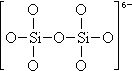 ,每个四面体中心含有1个Si原子,硅原子位居该四面体中心,四个氧原子各占一个顶点,为无支链的单环状,Si2O76-只有硅氧键,通过共用氧原子的形式构成,所以它的空间结构图可表示为:
,每个四面体中心含有1个Si原子,硅原子位居该四面体中心,四个氧原子各占一个顶点,为无支链的单环状,Si2O76-只有硅氧键,通过共用氧原子的形式构成,所以它的空间结构图可表示为: ,
,故答案为:
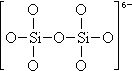 ;
; ;
;(3)甲醇分子之间形成氢键,沸点较高,甲醛(HCHO)中C原子形成3个σ键,碳原子轨道的杂化类型为sp2杂化,1mol甲醛分子中σ键的数目为3NA;轨道中电子处于全满、全空、半满时较稳定,所以气态Cu失去一个电子变成结构为[Ar]3d10的Cu+,能量较低,所以Cu的第二电离能相对较大(或气态Zn失去一个电子变成结构为[Ar]3d104s1的Zn+,易再失去一个电子,所以Zn的第二电离能相对较小),
故答案为:甲醇分子之间形成氢键;sp2杂化;3NA;Cu失去一个电子变成结构为[Ar]3d10的Cu+,属于能量较低稳定结构,所以Cu的第二电离能相对较大(或气态Zn失去一个电子变成结构为[Ar]3d104s1的Zn+,易再失去一个电子,所以Zn的第二电离能相对较小);
(4)沿X、Y、Z三轴切割的方法知,X轴上有2个氯离子,Y轴上有2个氯离子,Z轴上有2个氯离子,所以钠离子的配位数是6,将6个氯离子连接后所围成的空间几何构型正八面体,沿体对角线方向投影的几何形状为正六边形,晶体中每个Cl-同时吸引着6个Na+,每个钠离子同时吸引着6个氯离子,晶体中在每个Cl-周围与它最接近且距离相等的Cl-个数=3×8×
| 1 |
| 2 |
故答案为:正八面体;正六边形;9:10;
点评:本题考查较为综合,涉及电子排布式、晶胞的计算以及离子围成的空间构型等知识,需要学生具备扎实的基础与分析问题解决问题的能力,题目难度中等.

练习册系列答案
相关题目
下列解释实验事实的化学方程式正确的是( )
A、5mol Fe和4mol Cl2反应:5Cl2+4Fe
| ||||
| B、2mol KMnO4和3mol H2O2在酸性条件下反应:2MnO4-+3H2O2+6H+═Mn2++4O2↑+6H2O | ||||
| C、在电解液为氢氧化钾的甲醇燃料电池内电路中,阳极的电极反应式为:CH3OH-6e-+8OH-═CO32-+6H2O | ||||
| D、向NaAlO2溶液中通入过量CO2:CO2+3H2O+2AlO2-═2Al(OH)3↓+CO32- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、水电离出的c(H+)?c(OH-)=10-22的溶液:K+、Na+、SO42-、S2O32- |
| B、澄清透明溶液:Mg2+、Cu2+、Cl-、SO42- |
| C、使酚酞变红色的溶液:NH4+、K+、AlO2-、NO3- |
| D、含0.1mol?L-1 KI的溶液:Fe3+、Na+、NO3-、Cl- |
炼钢时常用的氧化剂是空气(或纯氧).炼钢过程中既被氧化又被还原的元素是( )
| A、铁 | B、硫 | C、氧 | D、碳 |
某反应的△H=+100kJ?mol-1,下列有关该反应的叙述正确的是( )
| A、正反应活化能不小于100kJ?mol-1 |
| B、正反应活化能小于100kJ?mol-1 |
| C、逆反应活化能一定小于100kJ?mol-1 |
| D、正反应活化能比逆反应活化能小100kJ?mol-1 |

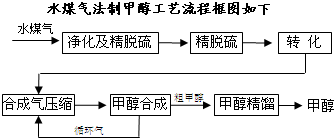 将煤气化转化成合成气,然后通过一碳化工路线合成各种油品和石化产品是一碳化工的极为重要的领域,具有广阔的前景,在未来相当一段时期将成为一碳化工的主要领域.
将煤气化转化成合成气,然后通过一碳化工路线合成各种油品和石化产品是一碳化工的极为重要的领域,具有广阔的前景,在未来相当一段时期将成为一碳化工的主要领域. 焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验: