题目内容
7.下列关于硫酸的说法正确的是( )| A. | 浓硫酸有脱水性,故可用做干燥剂 | |
| B. | 浓硫酸有强酸性,故能与金属活动顺序氢后的金属反应 | |
| C. | 硫酸的酸性比盐酸强,利用复分解反应用硫酸可以制盐酸 | |
| D. | 由于浓硫酸具强氧化性,因此不能干燥硫化氢和碘化氢气体 |
分析 A.依据浓硫酸有吸水性,故可用做干燥剂;
B.浓硫酸具有强的氧化性,能与金属活动顺序氢后的金属反应;
C.根据浓硫酸难挥发,盐酸易挥发分析;
D.浓硫酸具有强的氧化性,能够氧化硫化氢和碘化氢.
解答 解:A.浓硫酸有吸水性,故可用做干燥剂,不是脱水性,故A错误;
B.浓硫酸具有强的氧化性,能与金属活动顺序氢后的金属反应,故B错误;
C.浓硫酸难挥发,盐酸易挥发,则利用复分解反应用硫酸可以制盐酸,故C错误;
D.浓硫酸具有强的氧化性,能够氧化硫化氢和碘化氢,不能用浓硫酸干燥硫化氢和碘化氢,故D正确;
故选:D.
点评 本题考查了浓硫酸的性质,熟悉浓硫酸的强氧化性、脱水性、吸水性、难挥发性、酸性是解题关键,注意浓硫酸具有强的氧化性,不能用来制取还原性气体,例如硫化氢,碘化氢.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
8.下列有关σ键和π键的说法错误的是( )
| A. | 在某些分子中,化学键可能只有σ键而没有π键 | |
| B. | 分子中σ键的键能一定大于π键的键能 | |
| C. | σ键的特征是轴对称,π键的特征是镜面对称 | |
| D. | SO2形成π键与O3的π键是相似的 |
9.对下列物质的类別与所含官能团判断中,不正确的是( )
| A. | 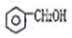 醇类-OH 醇类-OH | B. | CH3CH2COOH 羧酸类-COOH | ||
| C. | 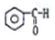 酮类-CHO 酮类-CHO | D. | CH3CH2Br 卤代烃类-Br |
15.滴定实验是化学学科中重要的定量实验.
已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下实验:
①称量1.0g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;
④用0.1000mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如表:
请回答下列问题:
(1)滴定终点时的现象是浅红色变为无色,30S不变色.
(2)所配制的250mL样品液中NaOH的物质的量浓度是0.08 mol•L-1;试样中NaOH的质量分数为80%.
(3)若出现下列情况,测定结果偏高的是ce.
a.滴定前用蒸馏水冲洗锥形瓶
b.在摇动锥形瓶时不慎将瓶内溶液溅出
c.滴定前有气泡,滴定后气泡消失
d.酸式滴定管滴至终点对,俯视读数
e.酸式滴定管用蒸馏水洗后,未用标准液润洗.
已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下实验:
①称量1.0g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;
④用0.1000mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如表:
| 滴定序号[来源:学科网] | 待测液体积(mL) | 所消耗标准盐酸的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 20.60 |
| 2 | 25.00 | 6.00 | 26.00 |
| 3 | 25.00 | 1.10 | 21.00 |
(1)滴定终点时的现象是浅红色变为无色,30S不变色.
(2)所配制的250mL样品液中NaOH的物质的量浓度是0.08 mol•L-1;试样中NaOH的质量分数为80%.
(3)若出现下列情况,测定结果偏高的是ce.
a.滴定前用蒸馏水冲洗锥形瓶
b.在摇动锥形瓶时不慎将瓶内溶液溅出
c.滴定前有气泡,滴定后气泡消失
d.酸式滴定管滴至终点对,俯视读数
e.酸式滴定管用蒸馏水洗后,未用标准液润洗.
12.下列关于铅蓄电池的说法正确的是( )
| A. | 放电时,正极电极反应是 Pb(s)+SO42-(aq)═PbSO4(s)+2e- | |
| B. | 放电时,电池的负极材料是铅板,负极质量增加 | |
| C. | 充电时,电池中硫酸的浓度始终保持不变 | |
| D. | 充电时,阳极发生的反应是 PbSO4(s)+2e-═Pb(s)+SO42-(aq) |
19.下列关于碱金属、卤族元素的说法正确的是( )
| A. | 碱金属单质的失电子能力随着原子序数的增加而减小 | |
| B. | 从上到下,卤素原子的电子层数依次增多,半径依次减小 | |
| C. | 从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱 | |
| D. | 碱金属单质都是强氧化剂 |
16.下列离子方程式正确的是( )
| A. | 向盐酸中加入适量氨水:H++OH-═H2O | |
| B. | 铁和稀硝酸反应:Fe+2H+═H2↑+Fe2+ | |
| C. | 在AlCl3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 铜与浓HNO3反应:3Cu+8H++2NO3-═3Cu2++4H2O+2NO↑ |
17.联苯的结构简式如右图( 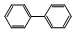 ),下列有关联苯的说法中正确的是( )
),下列有关联苯的说法中正确的是( )
 ),下列有关联苯的说法中正确的是( )
),下列有关联苯的说法中正确的是( )| A. | 它和蒽( 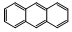 )同属于芳香烃,两者互为同系物 )同属于芳香烃,两者互为同系物 | |
| B. | 联苯的一氯代物有4种 | |
| C. | 1mol联苯最多可以和6molH2发生加成反应 | |
| D. | 它容易发生加成反应、取代反应,也容易被强氧化剂(如:酸性KMnO4溶液)氧化 |