题目内容
短周期元素X、Y、Z在周期表中的相对位置如图所示,下列判断正确的是( )
| X | ||
| Y | ||
| Z |
| A、X是最活泼的非金属元素 |
| B、Y的最高化合价为+7 |
| C、Z原子的最外层电子数是6 |
| D、3种元素的单质分子都是双原子分子 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:由如图所示的X、Y、Z三种主族元素在周期表中的相对位置可知,X、Y、Z三种主族元素处于过渡元素之后,X一定是第一周期元素,即X为He,Y为第二周期元素,为F,Z一定处于第三周期,为S,据此选择即可.
解答:
解:依据分析可知:X为He,Y为F,Z为S,
A、X为He是稀有气体元素,不活泼,故A错误;
B、Y为F,无最高价,故B错误;
C、Z为S,最外层电子数为6,故C正确;
D、He元素的单质为单原子分子,故D错误,故选C.
A、X为He是稀有气体元素,不活泼,故A错误;
B、Y为F,无最高价,故B错误;
C、Z为S,最外层电子数为6,故C正确;
D、He元素的单质为单原子分子,故D错误,故选C.
点评:考查元素周期表的结构、元素位置与结构关系,难度不大,要记住每一周期所含有元素的种类,利用上下周期元素的原子序数相互确定.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
质量分数为a%,物质的量浓度为cmol?L-1的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为( )
| A、等于2cmol?L-1 |
| B、大于2cmol?L-1 |
| C、小于2cmol?L-1 |
| D、在c~2cmol?L-1之间 |
已知H-H键能为436KJ/mol,H-N键能为391KJ/mol,根据化学方程式N2+3H2=2NH3△H=-92.4KJ/mol,则N≡N键的键能是( )
| A、431 KJ/mol |
| B、946 KJ/mol |
| C、649 KJ/mol |
| D、869 KJ/mol |
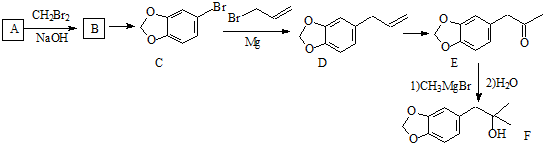
 系统命名为1-溴丙烯.
系统命名为1-溴丙烯.