题目内容
( 9分)对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含乙酸钠和对氯酚( )的废水可以通过构成微生物电池除去,其原理如下图所示。
)的废水可以通过构成微生物电池除去,其原理如下图所示。

①B是电池的 极(填“正”或“负”);②A极的电极反应式为 。
(2)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA ”表示乳酸分子,A-表示乳酸根离子)。
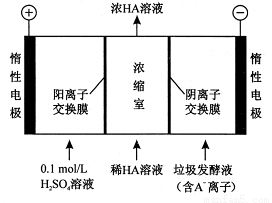
①阳极的电极反应式为 ;
②简述浓缩室中得到浓乳酸的原理 ;
③电解过程中,采取一定的措施可控制阳极室的pH约为6~8 ,此时进人浓缩室的OH-可忽略不计。400 mL10g/L 乳酸溶液通电一段时间后,浓度上升为 145g/L(溶液体积变化忽略不计),则阴极上产生的H2在标准状况下的体积约为 L(乳酸的摩尔质量为90g/ mol )。
(1)①负;②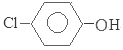 +H++2e-=
+H++2e-=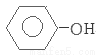 +Cl-;
+Cl-;
(2)①4OH--4e-=2H2O+O2↑;②阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室;A-通过阴离子交换膜从阴极进入浓缩室,H++A-=HA,乳酸浓度增大;③6.72
【解析】
试题分析:(1)①由于H+向A极板移动,根据同种电荷相互排斥,异种电荷相互吸引的原则,所以B是电池的负极;②A极的电极反应式为 +H++2e-=
+H++2e-= +Cl-;(2) ①在阳极溶液中的阴离子放电,由于OH-的放电能力大于含氧酸根离子,所以在阳极OH-放电,该电极的电极反应式为4OH--4e-=2H2O+O2↑;在阳极发生反应:2H++2e-=H2↑;②浓缩室中得到浓乳酸的原理是在阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室;A-通过阴离子交换膜从阴极进入浓缩室,H++A-=HA,所以乳酸浓度增大;③反应过程中产生的乳酸的质量是0.400 L(145g/L -10g/L)=54g.则乳酸的物质的量是54g÷90g/ mol=0.6mol;因为在反应过程乳酸根离子结合的H+离子的个数与反应过程中放电的H+或OH-的个数相等,所以n(H2)=1/2n(乳酸)=0.3mol,其在标准状况下体积是0.3mol×22.4L/mol=6.72L。
+Cl-;(2) ①在阳极溶液中的阴离子放电,由于OH-的放电能力大于含氧酸根离子,所以在阳极OH-放电,该电极的电极反应式为4OH--4e-=2H2O+O2↑;在阳极发生反应:2H++2e-=H2↑;②浓缩室中得到浓乳酸的原理是在阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室;A-通过阴离子交换膜从阴极进入浓缩室,H++A-=HA,所以乳酸浓度增大;③反应过程中产生的乳酸的质量是0.400 L(145g/L -10g/L)=54g.则乳酸的物质的量是54g÷90g/ mol=0.6mol;因为在反应过程乳酸根离子结合的H+离子的个数与反应过程中放电的H+或OH-的个数相等,所以n(H2)=1/2n(乳酸)=0.3mol,其在标准状况下体积是0.3mol×22.4L/mol=6.72L。
考点:考查电池电极的判断、电解原理的在废水处理中的应用和计算的知识。

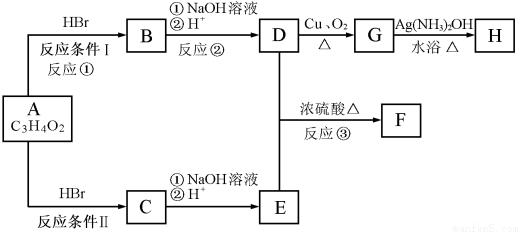
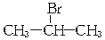 (主要产物),1 mol某芳香烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下面所示的一系列变化。
(主要产物),1 mol某芳香烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下面所示的一系列变化。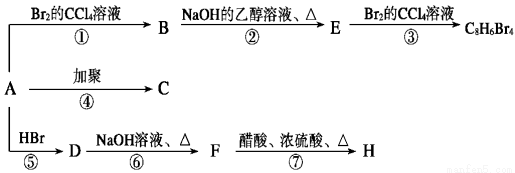
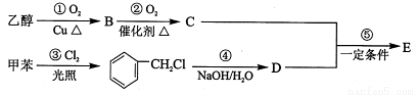
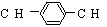 ,则M的结构式共有
,则M的结构式共有 
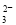 的水解程度和溶液的pH均增大
的水解程度和溶液的pH均增大