题目内容
2.常温下,分别将四块形状相同,质量均为6g的铁块同时投入下列四种溶液中,产生氢气速率最快的是( )| A. | 400mL 2mol/L HCl | B. | 300mL 2mol/L H2SO4 | ||
| C. | 100mL 3mol/L HNO3 | D. | 500mL 18.4mol/L H2SO4 |
分析 Fe与硝酸、浓硫酸反应不生成氢气,与盐酸、稀硫酸反应生成氢气,且氢离子浓度越大,反应速率越快,以此来解答.
解答 解:Fe与硝酸、浓硫酸反应不生成氢气,可排除C、D选项,A、B中氢离子浓度分别为2mol/L、2mol/L×2=4mol/L,则B中反应速率最快,
故选B.
点评 本题考查反应速率的影响因素,为高频考点,把握物质的性质、浓度对反应速率的影响为解答的关键,侧重分析与应用能力的考查,注意Fe与稀硫酸反应生成氢气,题目难度不大.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
8.下列反应属于取代反应的是( )
| A. | 乙醇与浓H2SO4共热170℃ | B. | 乙烯使溴水褪色 | ||
| C. | 甲苯与浓硫酸、浓硝酸混合 | D. | 苯与Cl2一定条件生成六氯环己烷 |
13.火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态N2O4.已知:①2O2(g)+N2(g)=N2O4(l)△H1 ②N2(g)+2H2(g)=N2H4(l)△H2 ③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=-1048kJ/mol
(1)上述反应热效应之间的关系式为△H4=2△H3-2△H2-△H1,
(2)又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态N2O4反应生成液态水时放出的热量是612kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是产物不会造成环境污染.
(4)合成氨工业中氢气可由天然气和水反应制备,其主要反应为:
CH4(g)+2H2O(g)?CO2(g)+4H2(g) 已知,破坏1mol化学键需要吸收的热量如表所示:
试通过计算得出该反应的△H=+162 kJ/mol.
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=-1048kJ/mol
(1)上述反应热效应之间的关系式为△H4=2△H3-2△H2-△H1,
(2)又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态N2O4反应生成液态水时放出的热量是612kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是产物不会造成环境污染.
(4)合成氨工业中氢气可由天然气和水反应制备,其主要反应为:
CH4(g)+2H2O(g)?CO2(g)+4H2(g) 已知,破坏1mol化学键需要吸收的热量如表所示:
| 化学键 | C-H | O-H | C=O | H-H |
| 吸收热量(kJ/mol) | 414 | 464 | 803 | 436 |
7.下列关于元素性质的有关叙述中不正确的是( )
| A. | S Cl 的原子半径依次减小 | |
| B. | Na Mg 的失电子能力依次增强 | |
| C. | O F的气态氢化物的稳定性依次增强 | |
| D. | Si P 的最高价含氧酸的酸性依次增强 |
14.下列变化中,属于加成反应的是( )
| A. | 乙炔通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色 | |
| B. | 甲苯在一定条件下与浓硝酸反应生成三硝基甲苯 | |
| C. | 乙醇在一定条件下与氢溴酸反应生成溴乙烷 | |
| D. | 在一定条件下苯与氢气反应制取环己烷 |
11. X、Y、Z、W均为短周期主族元素,其最高价氧化物对应水化物(常温下,浓度均为0.1mol•L-1)的pH和原子序数的关系如图所示.下列有关说法正确的是
X、Y、Z、W均为短周期主族元素,其最高价氧化物对应水化物(常温下,浓度均为0.1mol•L-1)的pH和原子序数的关系如图所示.下列有关说法正确的是
( )
 X、Y、Z、W均为短周期主族元素,其最高价氧化物对应水化物(常温下,浓度均为0.1mol•L-1)的pH和原子序数的关系如图所示.下列有关说法正确的是
X、Y、Z、W均为短周期主族元素,其最高价氧化物对应水化物(常温下,浓度均为0.1mol•L-1)的pH和原子序数的关系如图所示.下列有关说法正确的是( )
| A. | 简单离子半径:W>Z>Y>X | B. | 简单氢化物稳定性:X>Z>W | ||
| C. | 制造镁合金时可以用X2作保护气 | D. | 化合物Y2Z2中存在离子键和共价键 |
12.下列化合物的分子中,所有原子都处于同一平面的有( )
| A. | 乙烷 | B. | 甲苯 | C. | ClO3- | D. | SO3 |
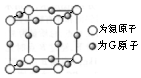 A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;D、E、F同周期;E核外的s、p能级的电子总数相筹;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.回答问题:
A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;D、E、F同周期;E核外的s、p能级的电子总数相筹;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.回答问题: