题目内容
有铁、氧化铁、四氧化三铁的混合物3.64克,加入50mL2mol/L盐酸溶液时,恰好完全反应,并且生成气体的体积在标准状况下为0.224升,向所得溶液中滴加KSCN溶液无明显变化.若将等质量的该混合物在CO中加热并充分反应,冷却后固体的质量为( )
| A、2 8克 |
| B、1.52克 |
| C、3.4克 |
| D、2克 |
考点:有关混合物反应的计算
专题:计算题
分析:盐酸恰好使混合物完全溶解,盐酸没有剩余,向反应所得溶液加KSCN溶液无血红色出现,说明溶液为FeCl2溶液,根据氯元素守恒可知n(FeCl2)=
n(HCl);用足量的CO在高温下还原相同质量的混合物得到铁,根据铁元素守恒可知n(Fe)=n(FeCl2),据此结合m=nM计算得到的铁的质量.
| 1 |
| 2 |
解答:
解:盐酸恰好使混合物完全溶解,盐酸没有剩余,向反应所得溶液加KSCN溶液无血红色出现,说明反应后的溶液为FeCl2溶液,根据氯元素守恒可知:n(FeCl2)=
n(HCl)=
×0.1L×1mol/L=0.05mol;
用足量的CO在高温下还原相同质量的混合物得到铁,根据铁元素守恒可知n(Fe)=n(FeCl2)=0.05mol,质量为:0.05mol×56g/mol=2.8g,
故选A.
| 1 |
| 2 |
| 1 |
| 2 |
用足量的CO在高温下还原相同质量的混合物得到铁,根据铁元素守恒可知n(Fe)=n(FeCl2)=0.05mol,质量为:0.05mol×56g/mol=2.8g,
故选A.
点评:本题考查混合物反应的计算,题目难度中等,根据体质信息正确判断反应后溶质组成为解答关键,注意守恒思想在化学计算中的运用,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
体积相同、pH相同的盐酸和醋酸溶液,再用氢氧化钠溶液中和时,两者消耗氢氧化钠的物质的量是( )
| A、相同 | B、盐酸多 |
| C、醋酸多 | D、无法比较 |
在相同状况下,将下列四种混合气体:①体积比为3:1的NH3和N2,②体积比为1:1的NO和NO2,③体积比为1:1的NO2和O2,④体积比为4:3的NO和O2.分别置于完全相同的试管里,并倒置与谁操着,充分反应后,液面上升的高度分别为h1 h2 h3 h4,下列关系正确的是( )
| A、h1>h2>h3>h4 |
| B、h4>h3>h1>h2 |
| C、h4>h1>h3>h2 |
| D、h2>h3>h1>h4 |
已知2X+O2→2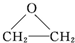 是原子利用率为100%的转化.下列对X的推断中不正确的是( )
是原子利用率为100%的转化.下列对X的推断中不正确的是( )
 是原子利用率为100%的转化.下列对X的推断中不正确的是( )
是原子利用率为100%的转化.下列对X的推断中不正确的是( )| A、可使酸性KMnO4溶液褪色 |
| B、可使溴水褪色 |
| C、一定条件下,可用H2除去乙烷中的X |
| D、与丙烯互为同系物 |
根据下表中所列出的数据,判断下列说法中正确的是( )
| 化学键 | 形成1mol化学键时放出的能量 |
| H-H | 436kJ |
| F-F | 157kJ |
| H-F | 568kJ |
| A、H2与F2反应的热化学方程式为H2(g)+F2(g)═2HF(g)△H=-543 kJ?mol-1 |
| B、2 L HF气体分解成1 L H2(g)和1 L F2(g)吸收543 kJ的热量 |
| C、1 mol H2(g)与1 mol F2(g)反应生成2 mol HF(l)放出的热量小于543 kJ |
| D、在相同条件下,1 mol H2(g)与1 mol F2(g)的总能量小于2 mol HF(g)的能量 |
 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示: