题目内容
12.为了加快漂白粉的作用,最好的方法是( )| A. | 加入苛性钠溶液 | B. | 用水湿润 | C. | 加少量盐酸 | D. | 加干燥剂使用 |
分析 漂白粉的有效成分的是次氯酸钙,但实际起漂白作用的是次氯酸,因此要加速漂白粉的漂白作用就得将次氯酸钙转化为次氯酸,利用强酸制弱酸的原理进行.
解答 解:根据漂白粉的成分是氯化钙和次氯酸钙的混合物,其有效成分为次氯酸钙,但实际上起漂白作用的是次氯酸,利用强酸制弱酸的原理,盐酸的酸性比比次氯酸的酸性强,次氯酸钙与盐酸反应生成具有漂白性的次氯酸,以加速漂白粉的漂白作用,加苛性钠、用水湿润、加热干燥,都不会产生次氯酸,
故选C.
点评 本题围绕漂白粉的漂白原理来分析解决,实际上还是元素化合物的性质问题,需要掌握相关元素化合物的性质,题目难度不大.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
20.下表是现行的元素周期表,请按题中要求回答下列有关问题:
(1)115号元素X的位置第七周期第ⅤA族
(2)画出⑨的简单离子的结构示意图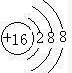 .
.
(3)①②⑤⑧的原子半径由大到小的顺序是Na>Si>C>H(用元素符号表示).
(4)②⑧⑨⑩的最高价氧化物的水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3>H2SiO3(用化学式表示).
(5)⑤与⑦的最高价氧化物的水化物间反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)⑨⑩的简单离子半径由大到小的顺序是S2->Cl-(用离子符号表示).
(7)⑩的非金属性比⑫强,用一个离子方程式表示为2Br-+Cl2=2Cl-+Br2.
(8)用电子式表示⑨与⑪形成化合物的过程为 .
.
(9)③的气态氢化物与其最高价含氧酸反应的产物中化学键的类型是离子键和共价键.
(10)⑥与⑦的金属性较强的是镁(填元素名称).
(11)②的最高价氧化物的电子式为 .
.
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||||||||||||
| ⑪ | ⑫ | ||||||||||||||||
(2)画出⑨的简单离子的结构示意图
 .
.(3)①②⑤⑧的原子半径由大到小的顺序是Na>Si>C>H(用元素符号表示).
(4)②⑧⑨⑩的最高价氧化物的水化物的酸性由强到弱的顺序是HClO4>H2SO4>H2CO3>H2SiO3(用化学式表示).
(5)⑤与⑦的最高价氧化物的水化物间反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)⑨⑩的简单离子半径由大到小的顺序是S2->Cl-(用离子符号表示).
(7)⑩的非金属性比⑫强,用一个离子方程式表示为2Br-+Cl2=2Cl-+Br2.
(8)用电子式表示⑨与⑪形成化合物的过程为
 .
.(9)③的气态氢化物与其最高价含氧酸反应的产物中化学键的类型是离子键和共价键.
(10)⑥与⑦的金属性较强的是镁(填元素名称).
(11)②的最高价氧化物的电子式为
 .
.
17.下列卤代烃发生消去后,可以得到两种烯烃( )
| A. | 1-氯丁烷 | B. | 氯乙烷 | C. | 2-氯丁烷 | D. | 溴丙烷 |
4.用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1L1mol/L的氯化铁溶液中,若C1-的数目为3 NA,则Fe3+的数目为NA | |
| B. | 1 molN2和3 molH2在一定条件下充分反应,转移电子数目为6NA | |
| C. | 常温下,1L0.1mol/L的Na2S溶液中阴离子数目大于0.1 NA | |
| D. | 0.1 mol Cl2通入水中,转移电子的数目为0.1NA |
1.高压下氮气聚合生成高聚氮,其晶体中每个氮原子都通过三个单键与其他氮原子结合并向空间发展构成立体网状结构.已知晶体中N-N键的键能为160KJ/mol,而N≡N的键能为942KJ/mol.则下列说法不正确的是( )
| A. | 键能越大说明化学键越牢固,所构成的物质越稳定 | |
| B. | 高聚氮晶体属于原子晶体 | |
| C. | 该晶体中氮原子数与氮氮键数比为1:3 | |
| D. | 高聚氮可以用作炸药 |
2.下列哪位科学家根据a粒子散射实验提出了原子结构的有核模型( )
| A. | 道尔顿 | B. | 卢瑟福 | C. | 汤姆生 | D. | 玻尔 |


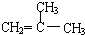 .
.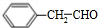 ;F分子中最多有15个原子共面.
;F分子中最多有15个原子共面.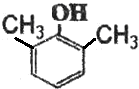 (或
(或 、
、 ).
).