题目内容
有关化学平衡常数(K)的说法中不正确的是( )
| A、K值越大,正反应进行的程度越大 |
| B、一般地说,K>105时,该反应进行得就基本完全了 |
| C、压强越大,K值越大 |
| D、K与反应物或生成物的浓度变化无关 |
考点:化学平衡常数的含义
专题:化学平衡专题
分析:平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,化学平衡常数只与温度有关,与浓度、压强无关,平衡常数越大,说明可逆反应进行的程度越大,以此解答该题.
解答:
解:A.K值越大,反应物的转化率越大,则正向反应进行的程度越大,故A正确;
B.一般地说,K>105时,该反应进行得就基本完全了,故B正确;
C.平衡常数是温度的函数,只与温度有关,对于同一个化学反应来说,在相同温度下,平衡常数为定值,压强越大,K值不变,故C错误;
D.平衡常数是温度的函数,只与温度有关,与物质浓度变化无关,故D正确;
故选C.
B.一般地说,K>105时,该反应进行得就基本完全了,故B正确;
C.平衡常数是温度的函数,只与温度有关,对于同一个化学反应来说,在相同温度下,平衡常数为定值,压强越大,K值不变,故C错误;
D.平衡常数是温度的函数,只与温度有关,与物质浓度变化无关,故D正确;
故选C.
点评:本题考查了化学平衡常数、影响因素及应用,为高频考点,侧重于学生的分析能力的考查,难度不大,注意化学平衡常数只与温度有关,同一转化关系化学计量数不同,平衡常数不同,温度相同,同一可逆反应的正、逆反应平衡常数互为倒数.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
实验室中有下列四组试剂,某同学欲分离含有KCl,MgCl2和BaCO3的混合物,应选用的试剂组是( )
| A、水,AgNO3溶液,稀HNO3 |
| B、水,KOH溶液,盐酸 |
| C、水,KOH溶液,稀HNO3 |
| D、水,NaOH溶液,盐酸 |
根据所学知识下列判断或处理不正确的是( )
| A、大量氯气泄漏时,现场人员可以用氢氧化钠溶液浸湿的毛巾蒙面,并迅速离开现场 |
| B、将浓硫酸沿烧杯内壁缓慢的注入水中稀释,同时用玻璃棒不断搅拌 |
| C、患有胃穿孔的病人胃酸过多,可以服用适量的含有氢氧化铝的胃药 |
| D、玻璃中含二氧化硅,盛装碳酸钠、氢氧化钠溶液的试剂瓶不能用玻璃塞 |
在科学史上,中国有许多重大的发明和发现,它们为世界的现代化奠定了基础,以下发明和发现属于化学史上中国对世界作出重大贡献的是( )
①火药 ②指南针 ③造纸 ④印刷术 ⑤炼铜、炼钢、炼铁 ⑥元素周期律的发现 ⑦人工合成蛋白 ⑧原子学说的提出.
①火药 ②指南针 ③造纸 ④印刷术 ⑤炼铜、炼钢、炼铁 ⑥元素周期律的发现 ⑦人工合成蛋白 ⑧原子学说的提出.
| A、②④⑥⑧ | B、①③⑤⑦ |
| C、④⑤⑦⑧ | D、①③④⑧ |
室温下等体积的NO和O2混合后混合气体平均分子量为( )
| A、30 | B、31 |
| C、41.33 | D、大于41.33 |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、pH=1的溶液中:NH4+、Na+、I-、NO3- |
| B、由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C、c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
| D、能使甲基橙变红的溶液中:NH4+、Al3+、NO3-、Cl- |
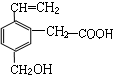 某有机物的结构简式如图.该物质不应有的化学性质是( )
某有机物的结构简式如图.该物质不应有的化学性质是( )①可燃烧
②可跟溴加成
③可使酸性KMnO4溶液褪色
④可跟NaHCO3溶液反应
⑤可跟NaOH溶液反应
⑥可在碱性条件下水解
⑦可与新制备的Cu(OH)2悬浊液煮沸生成红色沉淀.
| A、①② | B、③④ | C、④⑤ | D、⑥⑦ |
在澄清透明的强碱性溶液中,下列离子组能大量共存是( )
| A、Na+、H+、Cl- |
| B、Ba2+、Cl-、NO3- |
| C、K+、NH4+、CO32- |
| D、Na+、HCO3-、NO3- |