题目内容
将溶质的质量分数为a%、物质的量浓度为c1 mol·L-1的稀硫酸加热蒸发掉一定量的水,使溶质的质量分数变为2a%,此时硫酸的物质的量浓度为c2 mol·L-1,则c1和c2的关系是( )
A.c2=2c1 B.c2>2c1 C.c2<2cl D.c1=2c2
练习册系列答案
相关题目
2.有下有机物,请将它所对应的类别用序号填入下列表格中:
(1)CH3CH2CH3 ①酯
(2)CH2=CH-CH3 ②羧酸
(3)CH3COOCH3 ③醛
(4)CH3-CHO ④醇
(5)CH3-OH ⑤烯烃
(6)CH3CH2COOH ⑥烷烃
(1)CH3CH2CH3 ①酯
(2)CH2=CH-CH3 ②羧酸
(3)CH3COOCH3 ③醛
(4)CH3-CHO ④醇
(5)CH3-OH ⑤烯烃
(6)CH3CH2COOH ⑥烷烃
| 物质编号 | 所属类别编号 | 物质编号 | 所属类别编号 |
| (1) | (4) | ||
| (2) | (5) | ||
| (3) | (6) |
3.氢化钠(NaH)是一种白色的离子化合物.NaH与水反应放出氢气.下列叙述中正确的是( )
| A. | NaH中氢是+1价 | |
| B. | NaH中阴离子半径比锂离子半径小 | |
| C. | NaH中阴离子的电子层排布与氦原子相同 | |
| D. | NaH中阴离子可被还原成氢气 |
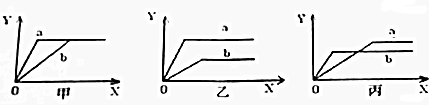
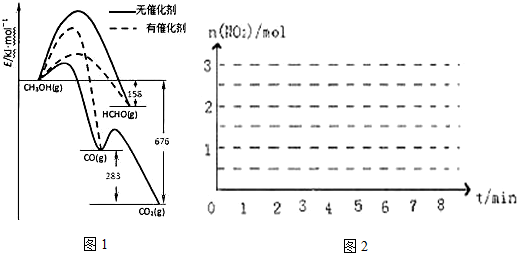
7.(1)(1)人们常用催化剂来选择反应进行的方向.如图1所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].
①写出1mol HCHO与O2反应主要生成CO和H2O(g)的热化学方程式:HCHO(g)+$\frac{1}{2}$O2(g)═CO(g)+H2O(g)△H=-235kJ•mol-1.
②CH3OH与O2在有催化剂作用下反应,产物中HCHO比率大大提高的原因是催化剂使生成HCHO的活化能降低,同时使生成CO的活化能升高,并且生成HCHO的活化能低于生成CO的活化能.
(2)①一定温度下,将N2H4与NO2以体积比为1:1置于容积固定的容器中发生反应2N2H4(g)+2NO2(g)?3N2(g)+4H2O(Ⅰ)△H<0,下列能说明反应达到平衡状态的是AD.
A.混合气体密度保持不变B.2vg正(NO2)=2v正(N2)
C.N2H4与NO2体积比保持不变D.体系压强保持不变
②在某温度下,10L密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
i.前2min内NO2的平均反应速率为0.025mol•L-1•min-1(保留2位有效数字,下同).
该温度下反应的平衡常数K8.4.
ii.关于上述反应,下列叙述不正确的是A.
A.达到平衡时,移走部分N2,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(N2H2)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入He,则此时v(逆)>v(正)
iii.请画出该反应中n(NO2)随时间变化曲线并画出在第7min时分别升温、加压的情况下n(NO2)随时间变化示意图(在图2上注明变化的条件).
①写出1mol HCHO与O2反应主要生成CO和H2O(g)的热化学方程式:HCHO(g)+$\frac{1}{2}$O2(g)═CO(g)+H2O(g)△H=-235kJ•mol-1.
②CH3OH与O2在有催化剂作用下反应,产物中HCHO比率大大提高的原因是催化剂使生成HCHO的活化能降低,同时使生成CO的活化能升高,并且生成HCHO的活化能低于生成CO的活化能.
(2)①一定温度下,将N2H4与NO2以体积比为1:1置于容积固定的容器中发生反应2N2H4(g)+2NO2(g)?3N2(g)+4H2O(Ⅰ)△H<0,下列能说明反应达到平衡状态的是AD.
A.混合气体密度保持不变B.2vg正(NO2)=2v正(N2)
C.N2H4与NO2体积比保持不变D.体系压强保持不变
②在某温度下,10L密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
| 物质的量/mol 时间 | n(N2H4) | N(NO2) | N(N2) |
| 起始 | 2.0 | 3.0 | 0 |
| 第2min | 1.5 | a | 0.75 |
| 第4min | 1.2 | b | 1.2 |
| 第6min | 1.0 | c | 1.5 |
| 第7min | 1.0 | c | 1.5 |
该温度下反应的平衡常数K8.4.
ii.关于上述反应,下列叙述不正确的是A.
A.达到平衡时,移走部分N2,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(N2H2)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入He,则此时v(逆)>v(正)
iii.请画出该反应中n(NO2)随时间变化曲线并画出在第7min时分别升温、加压的情况下n(NO2)随时间变化示意图(在图2上注明变化的条件).

4.下列关于金属的一些说法不正确的是( )
| A. | 合金的性质与其成分金属的性质不完全相同 | |
| B. | 工业上金属Mg、Al都是用电解熔融的氯化物制得的 | |
| C. | 黑色的氧化铜灼烧会变成砖红色 | |
| D. | 将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿 |