题目内容
铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)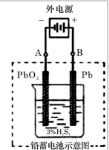
(1)放电时:正极的电极反应式是 ,电解液中H2SO4的浓度将变 ,当外电路通过1mol电子时,理论上负极板的质量增加 g.
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成 ,B电极上生成 ,此时铅蓄电池的正负极的极性将 .

(1)放电时:正极的电极反应式是
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成
考点:原电池和电解池的工作原理
专题:
分析:(1)电池总反应式为:Pb+PbO2+4H++2SO42-
2PbSO4+2H2O,写出电极反应为:负极电解反应:Pb-2e-+SO42-=PbSO4 ,正极电极反应:PbO2+2e-+4H++SO42-=PbSO4+2H2O,依据电解反应和电池原理分析判断;
(2)装置中使电解装置,电极上是析出的硫酸铅,所以是铅蓄电池的充电过程,依据电解原理分析.
| 放电 |
| 充电 |
(2)装置中使电解装置,电极上是析出的硫酸铅,所以是铅蓄电池的充电过程,依据电解原理分析.
解答:
解:(1)电池总反应式为:Pb+PbO2+4H++2SO42-
2PbSO4+2H2O,放电时,负极电极反应为Pb-2e-+SO42-=PbSO4 ,正极电极反应为PbO2+2e-+4H++SO42-=PbSO4+2H2O,由方程式可知反应消耗硫酸,则电解液中H2SO4的浓度将减少;当外电路通过1mol电子时,依据电子守恒计算理论上负极板的质量增加0.5mol×303g/mol-0.5mol×207g/mol=48g;
故答案为:PbO2+2e-+4H++SO42-=PbSO4+2H2O;小;48;
(2)在完全放电耗尽PbO2和Pb时,电极上是析出的PbSO4,若按题右图连接B为阳极应是失去电子发生氧化反应,A为阴极是得到电子发生还原反应,实质是电解反应,B电极上发生反应为:PbSO4+2H2O-2e-=PbO2+4H++2SO42-,A电极发生反应为:PbSO4=Pb-2e-+SO42-,所以A电极上生成Pb;B极生成PbO2,此时铅蓄电池的正负极的极性将对换,
故答案为:Pb; PbO2;对换.
| 放电 |
| 充电 |
故答案为:PbO2+2e-+4H++SO42-=PbSO4+2H2O;小;48;
(2)在完全放电耗尽PbO2和Pb时,电极上是析出的PbSO4,若按题右图连接B为阳极应是失去电子发生氧化反应,A为阴极是得到电子发生还原反应,实质是电解反应,B电极上发生反应为:PbSO4+2H2O-2e-=PbO2+4H++2SO42-,A电极发生反应为:PbSO4=Pb-2e-+SO42-,所以A电极上生成Pb;B极生成PbO2,此时铅蓄电池的正负极的极性将对换,
故答案为:Pb; PbO2;对换.
点评:本题考查了原电池原理,会根据电池反应式及元素化合价变化书写正负极电极反应式,再结合各个物理量之间的关系式进行计算,注意:负极上生成难溶性的硫酸铅导致负极质量增加,题目难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
下列说法或做法正确的是( )
| A、CO2通入可溶性硅酸盐中析出硅酸沉淀,所以硅酸的酸性小于碳酸 |
| B、金属钠着火燃烧时,用q灭火 |
| C、铝比铁活泼,所以铝比铁更容易被腐蚀 |
| D、正常雨水PH等于7,酸雨的PH小于7 |
常温常压下,现有浓度为0.100mol/L的六种溶液:①HCl,②H2SO4,③CH3COOH,④CH3COONa ⑤NaOH,⑥Na2CO3由水电离出的C(H+)大小关系正确的是( )
| A、⑥>④>③>①=⑤>② |
| B、①=②>③>⑥>④>⑤ |
| C、②>①>③>④>⑥>⑤ |
| D、④>⑥>③>①=⑤>② |
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-═ZnO+H2O Ag2O+H2O+2e-═2Ag+2OH-总反应为Ag2O+Zn═2Ag+ZnO.根据上述反应式,判断下列叙述中,正确的是( )
| A、在使用过程中,电池负极区溶液pH增大 |
| B、在使用过程中,电流由Ag2O极经外电路流向Zn极 |
| C、在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 |
| D、外电路中每通过0.2mol电子,正极的质量理论上减小33.2g |
萃取在生产和科学实验中有着广泛应用.下列混合物的分离中,需要应用萃取这种分离方法的是( )
| A、海水淡化 |
| B、分离豆浆和豆渣 |
| C、用海水晒盐 |
| D、从碘水中提取碘 |
下列有关烃的系统命名正确的有( )
| A、2,3-二甲基-3,3-二乙基戊烷 |
| B、2,3-二甲基丁烷 |
| C、2,2-二甲基-1-丁醇 |
| D、1,3-二甲基-1-丁醇 |

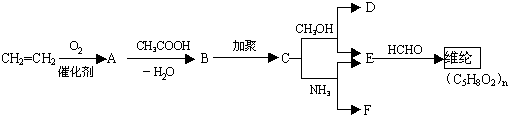
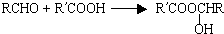 ,又知醇和氨都有似水性(与水的性质相似),酯可以水解又可以醇解或者氨解.现以乙烯为原料合成维纶,其主要步骤如下:
,又知醇和氨都有似水性(与水的性质相似),酯可以水解又可以醇解或者氨解.现以乙烯为原料合成维纶,其主要步骤如下: