题目内容
8.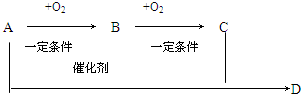 根据如图有机物的转化关系回答.已知A是乙醇.
根据如图有机物的转化关系回答.已知A是乙醇.(1)B、C、D的名称分别是乙醛、乙酸、乙酸乙酯.
(2)B转化成C的反应化学方程式2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.
分析 A是乙醇,乙醇在一定条件下氧化可得B为乙醛,B氧化得C为乙酸,乙醇和乙酸反应可以生成D为乙酸乙酯,据此答题.
解答 解:A是乙醇,乙醇在一定条件下氧化可得B为乙醛,B氧化得C为乙酸,乙醇和乙酸反应可以生成D为乙酸乙酯,
(1)根据上面的分析可知,B为乙醛,C为乙酸,D为乙酸乙酯,
故答案为:乙醛;乙酸;乙酸乙酯;
(2)B转化成C的反应为乙醛的催化氧化,反应的化学方程式为2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH,
故答案为:2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.
点评 本题考查有机物的推断,题目难度不大,注意有机物的官能团的相互转化和性质,注重基础知识的考查.

练习册系列答案
相关题目
13.2015年初,全国范围内遭遇了严重的雾霾天气,为了改善空气质量,政府提出减少化石能源的使用,提倡新能源,国家大力扶持光电产业,下列说法错误的是( )
| A. | 光伏发电主要利用高纯度单质硅制成的硅太阳能电池 | |
| B. | 硅太阳能电池可将太阳能直接转化为电能,减少化石燃料的使用,保护环境 | |
| C. | 硅的结构和金刚石类似,是具有金属光泽的灰黑色固体 | |
| D. | 硅单质即能与氢氧化钠反应又能与氢氟酸反应,所以硅是两性 |
17.能源、材料已成为当今科学研究的热点.请回答下列问题:
(1)单质A的燃烧热大,可作燃料.已知A为短周期元素,其气态原子逐个失去1~4个电子所需能量(电离能)如表所示.若该原子核外电子有三层,则该元素位于周期表ⅡA族,写出A燃烧后形成的氧化物的电子式: .
.

(2)如图是超导材料元素在周期表中的分布,上述元素的短周期元素中原子半径最大的是Al(填元素符号),其原子最外层有3种运动状态不同的电子,写出其最高价氧化物对应水化物在水溶液中的电离方程式:H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
(3)上述主族元素中有两种原子可以形成的五核分子,其化学键键长和键角都相等,则该分子的空间构型为正四面体,该物质为非极性分子(选填“极性”或“非极性”).
(4)铁单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,且每生成1mol该易燃气体放出37.68kJ热量,请写出此反应的热化学方程式:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2 (g)△H=-150.72kJ/mol.
(5)取适量Al、Mg合金样品置于烧杯中,加入20mL 1mol/L的NaOH溶液,恰好完全反应.下列叙述正确的是b(选填编号).
a.Mg作负极,Al作正极
b.若加入的是20mL 1mol/L的盐酸,则放出的氢气的物质的量减少$\frac{2}{3}$
c.若把NaOH中的H换成D(D为重氢),生成的氢气中D与H物质的量之比为1:2.
(1)单质A的燃烧热大,可作燃料.已知A为短周期元素,其气态原子逐个失去1~4个电子所需能量(电离能)如表所示.若该原子核外电子有三层,则该元素位于周期表ⅡA族,写出A燃烧后形成的氧化物的电子式:
 .
.| I1 | I2 | I3 | I4 | … | |
| 电离能(kJ/mol) | 738 | 1451 | 7733 | 10540 | … |

(2)如图是超导材料元素在周期表中的分布,上述元素的短周期元素中原子半径最大的是Al(填元素符号),其原子最外层有3种运动状态不同的电子,写出其最高价氧化物对应水化物在水溶液中的电离方程式:H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
(3)上述主族元素中有两种原子可以形成的五核分子,其化学键键长和键角都相等,则该分子的空间构型为正四面体,该物质为非极性分子(选填“极性”或“非极性”).
(4)铁单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,且每生成1mol该易燃气体放出37.68kJ热量,请写出此反应的热化学方程式:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2 (g)△H=-150.72kJ/mol.
(5)取适量Al、Mg合金样品置于烧杯中,加入20mL 1mol/L的NaOH溶液,恰好完全反应.下列叙述正确的是b(选填编号).
a.Mg作负极,Al作正极
b.若加入的是20mL 1mol/L的盐酸,则放出的氢气的物质的量减少$\frac{2}{3}$
c.若把NaOH中的H换成D(D为重氢),生成的氢气中D与H物质的量之比为1:2.
18.下表为周期表中短周期的一部分,若R原子核外有3个未成对电子,说法正确的是( )
| R | ||
| X | Y | Z |
| A. | 原子半径大小顺序是:Y>X>R | |
| B. | 其气态氢化物的稳定性顺序是:Z>Y>X>R | |
| C. | X、Y、Z中Z的氧化物对应的水化物的酸性最强 | |
| D. | R的气态氢化物与它的含氧酸之间能发生化学反应 |