题目内容
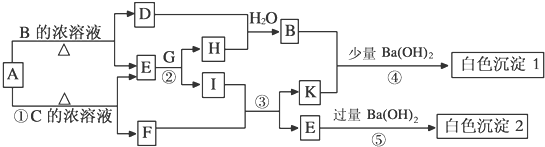
已知:A~K物质之间的转化关系如图所示,D、E、F、H均为气体,其中E、F、H为无色气体,A为形成化合物种类最多的元素形成的单质,G为黄色粉末(部分产物未给出).
根据题意回答下列问题:
(1)写出下列物质的化学式:
D ;白色沉淀1: ;白色沉淀2: .
(2)写出①、②反应的化学方程式:
① ,
② ,
②反应可用于 .
(3)I溶液呈 性(填“酸”、“碱”或“中”),升高温度,该溶液的pH (填“增大”、“减小”或“不变”),原因是 .
(写出离子方程式和必要的文字说明).
(4)若K为等物质的量的F与I反应的产物,将B与过量的Ba(OH)2混合后加入K,所得白色沉淀为 .

根据题意回答下列问题:
(1)写出下列物质的化学式:
D
(2)写出①、②反应的化学方程式:
①
②
②反应可用于
(3)I溶液呈
(写出离子方程式和必要的文字说明).
(4)若K为等物质的量的F与I反应的产物,将B与过量的Ba(OH)2混合后加入K,所得白色沉淀为
考点:无机物的推断
专题:推断题
分析:由题干信息可知A为碳,G为Na2O2,有色气体D只能是NO2,能与碳反应生成NO2的B必是HNO3,因此E为CO2,碳与C的浓溶液加热也能产生CO2,则C必是H2SO4,故F是SO2,以此可推断框图中的其它物质,H为O2,I为Na2CO3,K为Na2SO3或NaHSO3,它与HNO3混合后,被HNO3氧化生成SO42-,与Ba(OH)2反应生成白色沉淀1为BaSO4,CO2与过量Ba(OH)2反应生成白色沉淀2为BaCO3,若K为等物质的量的SO2与Na2CO3反应的产物,则SO2+Na2CO3═Na2SO3+CO2,K为Na2SO3,HNO3与Ba(OH)2(过量)反应生成Ba(NO3)2,Ba(NO3)2与Na2SO3反应可生成沉淀BaSO3.
解答:
解:由题干信息可知A为碳,G为Na2O2,有色气体D只能是NO2,能与碳反应生成NO2的B必是HNO3,因此E为CO2,碳与C的浓溶液加热也能产生CO2,则C必是H2SO4,故F是SO2,以此可推断框图中的其它物质,H为O2,I为Na2CO3,K为Na2SO3,它与HNO3混合后,被HNO3氧化生成SO42-,与Ba(OH)2反应生成白色沉淀1为BaSO4,CO2与过量Ba(OH)2反应生成白色沉淀2为BaCO3,若K为等物质的量的SO2与Na2CO3反应的产物,则SO2+Na2CO3═Na2SO3+CO2,K为Na2SO3,HNO3与Ba(OH)2(过量)反应生成Ba(NO3)2,Ba(NO3)2与Na2SO3反应可生成沉淀BaSO3,判断沉淀2为BaSO3;
(1)上述分析可知D为NO2,沉淀1为BaSO4,沉淀2为BaCO3,故答案为:NO2;BaSO4;BaCO3;
(2)反应①是碳和浓硫酸加热反应生成二氧化碳、二氧化硫和水,反应的化学方程式为:C+2H2SO4(浓)
CO2↑+2SO2+2H2O;反应②为二氧化碳和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:2CO2+2Na2O2═2Na2CO3+O2;反应②过氧化钠和二氧化碳反应生成氧气,可以作为呼吸面具或潜水艇中作供氧剂;
故答案为:C+2H2SO4(浓)
CO2↑+2SO2+2H2O;2CO2+2Na2O2═2Na2CO3+O2;呼吸面具或潜水艇中作供氧剂;
(3)I溶液为Na2CO3溶液,碳酸根离子水解显碱性,CO32-+H2O?HCO3-+OH-,水解平衡时吸热过程,升温平衡正向进行,碱性增强,溶液PH增大,
故答案为:碱;增大;CO32-+H2O?HCO3-+OH-,升高温度水解平衡正向移动,碱性增强;
(4)等物质的量的F为SO2与I为Na2CO3反应的产物,SO2+Na2CO3═Na2SO3+CO2,K为Na2SO3,将B为HNO3与过量的Ba(OH)2混合后加入K,HNO3与Ba(OH)2(过量)反应生成Ba(NO3)2,Ba(NO3)2与Na2SO3反应可生成沉淀BaSO3.所得白色沉淀BaSO3,故答案为:BaSO3.
(1)上述分析可知D为NO2,沉淀1为BaSO4,沉淀2为BaCO3,故答案为:NO2;BaSO4;BaCO3;
(2)反应①是碳和浓硫酸加热反应生成二氧化碳、二氧化硫和水,反应的化学方程式为:C+2H2SO4(浓)
| ||
故答案为:C+2H2SO4(浓)
| ||
(3)I溶液为Na2CO3溶液,碳酸根离子水解显碱性,CO32-+H2O?HCO3-+OH-,水解平衡时吸热过程,升温平衡正向进行,碱性增强,溶液PH增大,
故答案为:碱;增大;CO32-+H2O?HCO3-+OH-,升高温度水解平衡正向移动,碱性增强;
(4)等物质的量的F为SO2与I为Na2CO3反应的产物,SO2+Na2CO3═Na2SO3+CO2,K为Na2SO3,将B为HNO3与过量的Ba(OH)2混合后加入K,HNO3与Ba(OH)2(过量)反应生成Ba(NO3)2,Ba(NO3)2与Na2SO3反应可生成沉淀BaSO3.所得白色沉淀BaSO3,故答案为:BaSO3.
点评:本题考查了物质转化关系,物质性质的分析判断,主要是钠、氮及其化合物性质的理解应用,注意反应实质和反应产物的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
下列关于有机物的说法中错误的是( )
| A、甲苯、葡萄糖和乙醇均能使酸性高锰酸钾溶液褪色 |
| B、在鸡蛋白溶液中加入浓Na2SO4溶液,蛋白质发生变性 |
| C、乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
| D、分子式为C7H8O属于芳香族化合物的同分异构体有5种 |
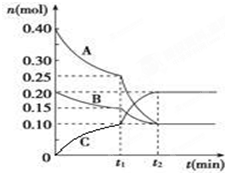 现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图:
现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图: