题目内容
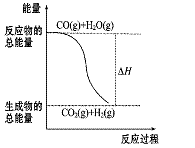
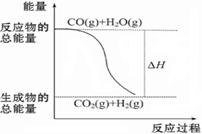
燃烧热是指一定条件下1 mol可燃物完全燃烧生成稳定的氧化物时放出的热量。已知热化学方程式:①CO(g)+1/2 O2(g)====CO2(g)ΔH = -283.0 kJ·mol-1
②H2(g)+ 1/2O2(g)====H2O(g)ΔH = -241.8 kJ·mol-1
则下列说法正确的是( )
|
B. H2的燃烧热为241.8 kJ·mol-1
C.H2(g)转变成H2O(g)的化学反应一定要释放能量
D.根据②推知反应H2(g)+1/2O2(g)==== H2O(l)
ΔH > -241.8 kJ·mol-1
A

练习册系列答案
相关题目
燃烧热是指一定条件下1 mol可燃物完全燃烧生成稳定的氧化物时放出的热量。已知热化学方程式:①CO(g)+1/2 O2(g)====CO2(g)ΔH =" -283.0" kJ·mol-1
②H2(g)+ 1/2O2(g)====H2O(g)ΔH =" -241.8" kJ·mol-1
则下列说法正确的是( )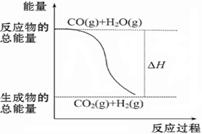
| A.由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)="===" CO2(g)+H2(g)ΔH =" -41.2" kJ·mol-1 |
| B.H2的燃烧热为241.8 kJ·mol-1 |
| C.H2(g)转变成H2O(g)的化学反应一定要释放能量 |
| D.根据②推知反应H2(g)+1/2O2(g)="===" H2O(l)ΔH > -241.8 kJ·mol-1 |