题目内容
下列反应的离子方程式书写正确的是( )
| A、Na2O2溶于水:O22-+H2O=2OH-+O2↑ |
| B、向水玻璃中加入少量醋酸:SiO32-+2H+=H2SiO3(胶体) |
| C、澄清石灰水中滴加过量NaHCO3溶液:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
| D、磁性氧化铁溶于足量的浓盐酸:Fe3O4+8H+=3Fe3++4H2O |
考点:离子方程式的书写
专题:
分析:A.过氧化钠在离子反应中保留化学式;
B.醋酸在离子反应中保留化学式;
C.石灰水完全反应,生成碳酸钙、碳酸钠和水;
D.反应生成氯化铁、氯化亚铁、水.
B.醋酸在离子反应中保留化学式;
C.石灰水完全反应,生成碳酸钙、碳酸钠和水;
D.反应生成氯化铁、氯化亚铁、水.
解答:
解:A.Na2O2溶于水的离子反应为2Na2O2+2H2O=4OH-+4Na++O2↑,故A错误;
B.向水玻璃中加入少量醋酸的离子反应为SiO32-+2CH3COOH=H2SiO3(胶体)+2CH3COO-,故B错误;
C.澄清石灰水中滴加过量NaHCO3溶液的离子反应为Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O,故C正确;
D.磁性氧化铁溶于足量的浓盐酸的离子反应为Fe3O4+8H+=2Fe3++Fe2++4H2O,故D错误;
故选C.
B.向水玻璃中加入少量醋酸的离子反应为SiO32-+2CH3COOH=H2SiO3(胶体)+2CH3COO-,故B错误;
C.澄清石灰水中滴加过量NaHCO3溶液的离子反应为Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O,故C正确;
D.磁性氧化铁溶于足量的浓盐酸的离子反应为Fe3O4+8H+=2Fe3++Fe2++4H2O,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应、与量有关的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
有四种化合物:①NaHCO3 ②Al(OH)3 ③Al ④Al2O3,既能和盐酸反应,又能和NaOH溶液反应的物质有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、4.6 g Na完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1 NA |
| B、标准状况下,11.2L Cl2与足量的铁反应转移的电子数为NA |
| C、将100mL 0.1mol?L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA |
| D、物质的量浓度为0.5 mol/L的NaCl溶液中,含有Cl-个数为0.5NA |
下列关于“物质的量”、“摩尔”和“摩尔质量”的叙述中正确的是( )
| A、物质的摩尔质量等于其相对分子(原子)质量 |
| B、0.012 kg 12C中所含的碳原子数为NA |
| C、“物质的量”是国际单位制中的一个基本单位 |
| D、1mol任何物质都含有约6.02×1023个原子 |
不属于氮的固定的变化是( )
| A、氨催化氧化制硝酸 |
| B、由氮气和氢气合成氨气 |
| C、镁条在氮气中燃烧 |
| D、豆科植物的根瘤固氮 |
羟基自由基可以看做是氢氧根离子失去一个电子后形成的,具有极强的得电子能力,用于有机废水的处理.关于羟基自由基的说法正确的是( )
A、电子式 |
B、电子式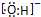 |
| C、有极强的还原性 |
| D、与NH3所含电子数相同 |


