题目内容
16.下列叙述正确的是( )| A. | 强电解质都是离子化合物,因此NaCl是离子化合物 | |
| B. | 亚硫酸溶液的导电能力可能比稀硫酸强 | |
| C. | SO3溶于水,其水溶液能导电,SO3是电解质 | |
| D. | 石墨是单质,能导电,因此石墨是电解质 |
分析 A.强电解质不一定是离子化合物;
B.溶液的导电能力主要由溶液中的离子浓度决定;
C.在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里或熔融状态下都不导电的化合物是非电解质;
D.电解质和非电解质都是化合物.
解答 解:A.强电解质不一定是离子化合物,HCl是强电解质但是共价化合物,故A错误;
B.溶液的导电能力主要由溶液中的离子浓度决定,亚硫酸溶液部分电离,但电离出来的离子浓度可能比硫酸电离出来的大,故B正确;
C.SO3和水反应生成硫酸,硫酸能电离出自由移动的阴阳离子,所以SO3的水溶液导电,但电离出离子的物质是硫酸不是SO3,所以SO3是非电解质,故C错误;
D.石墨是单质,既不是电解质也不是非电解质,故D错误.
故选B.
点评 本题考查强电解质和弱电解质,电解质和非电解质,题目难度不大,平时注意知识的积累.

练习册系列答案
相关题目
6.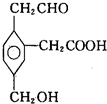 某有机物的结构简式如图所示,在一定条件下对于下列反应:
某有机物的结构简式如图所示,在一定条件下对于下列反应:
①加成、②水解、③酯化、④氧化、⑤中和、⑥消去,其中该物质可能发生的是( )
 某有机物的结构简式如图所示,在一定条件下对于下列反应:
某有机物的结构简式如图所示,在一定条件下对于下列反应:①加成、②水解、③酯化、④氧化、⑤中和、⑥消去,其中该物质可能发生的是( )
| A. | ②③④ | B. | ①③④⑤ | C. | ①③⑤⑥ | D. | ②③④⑤⑥ |
4.等物质的量的下列有机物,充分燃烧耗氧量最大的是( )
| A. | C3H8 | B. | C2H6O | C. | C4H8O | D. | C4H8O2 |
11.Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2、NO三者的物质的量之比为2:1时,实际参加反应的Cu2S与HNO3的物质的量之比为( )
| A. | 1:8 | B. | 1:6 | C. | 1:5 | D. | 1:10 |
8.1861年德国人基尔霍夫(G.R.Kirchhoff)和本生(R.W.Bunsen)研究锂云母的某谱时,发现在深红区有一新线,从而发现了铷元素,他们研究的某谱是( )
| A. | 原子光谱 | B. | 质谱 | C. | 红外光谱 | D. | 核磁共振谱 |
5.X元素的原子序数是9,下列哪一原子序数的元素与X具有相似的化学性质( )
| A. | 1 | B. | 8 | C. | 17 | D. | 18 |
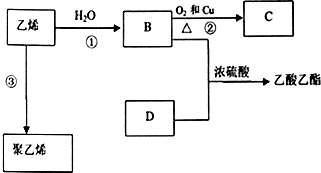 已知乙烯能发生以下转化:
已知乙烯能发生以下转化: .
.