题目内容
高铁酸钠(Na2FeO4)可以对饮用水进行净化处理,可由下列方法制得:Fe2O3+3Na2O2
2Na2FeO4+Na2O,关于该反应说法正确的是( )
| ||
| A、Na2FeO4属于共价化合物 |
| B、反应中Na2O2是氧化剂 |
| C、生成1 mol Na2FeO4,有6 mol 电子转移 |
| D、在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌 |
考点:氧化还原反应
专题:
分析:该反应中Fe元素化合价由+3价变为+6价、过氧化钠中O元素化合价由-1价变为-2价,所以氧化铁是还原剂、过氧化钠是氧化剂,再结合物质之间的转化计算.
解答:
解:该反应中Fe元素化合价由+3价变为+6价、过氧化钠中O元素化合价由-1价变为-2价,所以氧化铁是还原剂、过氧化钠是氧化剂,
A.Na2FeO4中钠离子和高铁酸根离子之间存在离子键,属于离子化合物,故A错误;
B.通过以上分析知,反应中Na2O2是氧化剂,故B正确;
C.生成1 mol Na2FeO4,转移电子的物质的量=1mol×(6-3)=3mol,故C错误;
D.在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌,故D错误;
故选B.
A.Na2FeO4中钠离子和高铁酸根离子之间存在离子键,属于离子化合物,故A错误;
B.通过以上分析知,反应中Na2O2是氧化剂,故B正确;
C.生成1 mol Na2FeO4,转移电子的物质的量=1mol×(6-3)=3mol,故C错误;
D.在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌,故D错误;
故选B.
点评:本题考查氧化还原反应,侧重考查基本概念、计算,明确元素化合价变化是解本题关键,注意高铁酸钠能杀菌消毒,题目难度不大.

练习册系列答案
相关题目
某有机物 的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )
的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )
 的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )
的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )| A、3种 | B、4 种 |
| C、5种 | D、6种 |
分类是化学学习和研究中的常用手段,下列分类依据和结论都正确的是( )
| A、浓盐酸、浓硫酸、浓硝酸均具有氧化性,都属氧化性酸 |
| B、Na2O、SO2、BaSO4在熔融状态或溶于水时均能导电,都属电解质 |
| C、NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物 |
| D、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,分类标准是可溶于水 |
关于如图装置说法正确的是( )
A、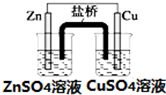 装置中,盐桥中的K+移向ZnSO4溶液 |
B、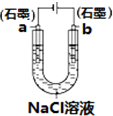 装置工作一段时间后,a极附近溶液的OH-的浓度增大 |
C、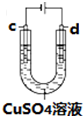 用装置精炼铜时,c极为粗铜 |
D、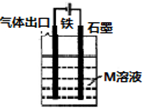 装置中若M是海水,该装置是通过“牺牲阳极保护法”使铁不被腐蚀 |
室温下,有两种溶液:①0.01mol?L-1NH3?H2O溶液、②0.01mol?L-1NH4Cl溶液,下列操作可以使两种溶液中c(NH4+)都增大的是( )
| A、通入少量HCl气体 |
| B、加入少量NaOH固体 |
| C、加入少量H2O |
| D、适当升高温度 |
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.01mol的酸性混合溶液中加入0.01mol铁粉,经搅拌后发生的变化应是( )
| A、铁溶解,析出0.01 mol Ag和0.005 mol Cu |
| B、铁溶解,析出0.01 mol Ag并放出H2 |
| C、铁溶解,析出0.01 mol Ag,溶液中不再有Fe3+ |
| D、铁溶解,析出0.01 mol Ag,溶液中不再有Cu2+ |
下列叙述正确的是( )
| A、元素周期表中位于金属与非金属分界线附近的元素属于过渡元素 |
| B、短周期第IVA族与VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
| C、C、N、O、H四种元素形成的化合物一定既有离子键又有共价键 |
| D、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、1molNa2O2固体中含有的阴阳离子总数为4NA |
| B、标准状况下,11.2L四氯化碳中含有的C-CI键的个数为2NA |
| C、1L1 mol?L-1的NaClO溶液中含有ClO-的数目为NA |
| D、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A、乙炔的结构简式:CHCH |
| B、乙酸乙酯的实验式C4H8O2 |
C、一氯甲烷的电子式: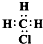 |
D、丙烷的球棍模型: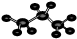 |