题目内容
 (2011?四川模拟)在1L密闭容器中,充入一定量的A发生反应:A(g)
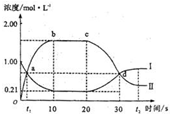
(2011?四川模拟)在1L密闭容器中,充入一定量的A发生反应:A(g)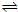 2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )
2B(g)(正反应为放热反应).当反应达到平衡后,改变影响平衡的一个条件,反应达到新的平衡.如图Ⅰ、Ⅱ两曲线分别表示整个反应过程中两种物质的浓度变化关系.下列说法正确的是( )分析:A、各物质的量的浓度不再发生变化说明反应到达平衡,a点和d点不是平衡状态.
B、a点时,A、B的浓度相等,A的起始浓度为1mol/L,令a点B的浓度为c,根据方程式A(g)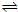 2B(g)可知A的浓度变化为0.5c,所以1-0.5c=c,据此计算判断.
2B(g)可知A的浓度变化为0.5c,所以1-0.5c=c,据此计算判断.
C、由图可知20s~t2s,B的浓度减小,A的浓度增大.若降低温度使平衡移动,反应为放热反应,降低温度平衡向正反应移动,B的浓度应该增大,A的浓度应增大,据此判断.
D、由图可知0s~10s,A的浓度变化为0.79mol/L,根据c=
计算v(A),再根据速率之比等于化学计量数之比计算v(B).
B、a点时,A、B的浓度相等,A的起始浓度为1mol/L,令a点B的浓度为c,根据方程式A(g)
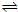 2B(g)可知A的浓度变化为0.5c,所以1-0.5c=c,据此计算判断.
2B(g)可知A的浓度变化为0.5c,所以1-0.5c=c,据此计算判断.C、由图可知20s~t2s,B的浓度减小,A的浓度增大.若降低温度使平衡移动,反应为放热反应,降低温度平衡向正反应移动,B的浓度应该增大,A的浓度应增大,据此判断.
D、由图可知0s~10s,A的浓度变化为0.79mol/L,根据c=
| △c |
| △t |
解答:解:A、a点和d点反应混合物的浓度还在发生变化,不是平衡状态,故A错误;
B、a点时,A、B的浓度相等,A的起始浓度为1mol/L,令a点B的浓度为c,根据方程式A(g)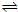 2B(g)可知A的浓度变化为0.5c,所以1mol/L-0.5c=c,解得c=0.67mol/L,故B正确;
2B(g)可知A的浓度变化为0.5c,所以1mol/L-0.5c=c,解得c=0.67mol/L,故B正确;
C、由图可知20s~t2s,B的浓度减小,A的浓度增大.若降低温度使平衡移动,反应为放热反应,降低温度平衡向正反应移动,B的浓度应该增大,A的浓度应增大,故不可能是降低温度,应为升高温度,故C错误;
D、由图可知0s~10s,A的浓度变化为1mol/L-0.21mol/L=0.79mol/L,所以v(A)=
0.079mol/(L?mol),速率之比等于化学计量数之比,所以v(B)=2v(A)=2×0.079mol/(L?mol)=0.158mol/(L?mol),故D错误.
故选:B.
B、a点时,A、B的浓度相等,A的起始浓度为1mol/L,令a点B的浓度为c,根据方程式A(g)
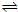 2B(g)可知A的浓度变化为0.5c,所以1mol/L-0.5c=c,解得c=0.67mol/L,故B正确;
2B(g)可知A的浓度变化为0.5c,所以1mol/L-0.5c=c,解得c=0.67mol/L,故B正确;C、由图可知20s~t2s,B的浓度减小,A的浓度增大.若降低温度使平衡移动,反应为放热反应,降低温度平衡向正反应移动,B的浓度应该增大,A的浓度应增大,故不可能是降低温度,应为升高温度,故C错误;
D、由图可知0s~10s,A的浓度变化为1mol/L-0.21mol/L=0.79mol/L,所以v(A)=
| 0.79mol/L |
| 10s |
故选:B.
点评:该题涉及化学平衡移动的影响因素和化学反应速率的有关计算.需读懂化学平衡的图象,解化学平衡图象题:一看轴,弄清横坐标和纵坐标的意义.二看点,弄清图象上点的意义,看起点,交点,转折点,终点.三看量的变化,

练习册系列答案
相关题目
 (2011?四川模拟)X、Y、Z是短周期元素,在周期表中的位置关系如图所示,下列说法不正确的是( )
(2011?四川模拟)X、Y、Z是短周期元素,在周期表中的位置关系如图所示,下列说法不正确的是( )