题目内容
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,16 g CH4中含有的原子总数为5NA |
| B、标准状况下,11.2 LCH3OH中含有的共价键数目为2.5NA |
| C、常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
| D、标准状况下,0.1 mol Cl2被氢氧化钠溶液完全吸收,转移的电子数目为0.2NA |
考点:阿伏加德罗常数
专题:
分析:A、求出甲烷的物质的量,然后根据1mol甲烷中含5mol原子来分析;
B、标况下,甲醇为液态;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、氯气与氢氧化钠的反应为歧化反应.
B、标况下,甲醇为液态;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、氯气与氢氧化钠的反应为歧化反应.
解答:
解:A、16g甲烷的物质的量n=
=1mol,而1mol甲烷中含5mol原子,故含有的原子的个数为5NA,故A正确;
B、标况下,甲醇为液态,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,故2.24 L CO和CO2混合气体的物质的量小于0.1mol,故含有的碳原子数小于0.1NA个,故C错误;
D、氯气与氢氧化钠的反应为歧化反应,1mol氯气转移1mol电子,故0.1mol氯气转移0.1mol电子,故D错误.
故选A.
| 16g |
| 16g/mol |
B、标况下,甲醇为液态,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,故2.24 L CO和CO2混合气体的物质的量小于0.1mol,故含有的碳原子数小于0.1NA个,故C错误;
D、氯气与氢氧化钠的反应为歧化反应,1mol氯气转移1mol电子,故0.1mol氯气转移0.1mol电子,故D错误.
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列高分子材料中属于线性结构的是( )
| A、聚丙烯 | B、硫化橡胶 |
| C、电木 | D、有机玻璃 |
下列用来表示物质变化的化学用语中,正确的是( )
| A、钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
| B、HS-的水解方程式:HS-+H2O?S2-+H3O+ |
| C、CO32-的水解方程式:CO32-+H2O?HCO3-+OH- |
| D、AlCl3溶液与Na2CO3溶液混合:2Al3++3CO32-═Al2(CO3)3↓ |
绿矾(FeSO4?7H2O)的相关性质如下图所示,反应①至⑥均在隔绝空气条件下进行,气体1、2、3的摩尔质量依次增大.

下列推断合理的是( )

下列推断合理的是( )
| A、能发生氧化还原反应的只有①、②、④、⑥ |
| B、将反应①和反应③产生的气体混合,气体颜色发生变化 |
| C、反应⑤生成的固体在空气中高温灼烧只发生分解反应 |
| D、将气体1和气体3冷凝再混合,能计算出所得溶液的物质的量浓度 |
设阿伏加德罗常数为NA,则下列说法正确的是( )
| A、11.2LNH3中含有的氢原子数为1.5NA |
| B、0.2mol/L的NaAlO2溶液含有0.2NA个Al3+ |
| C、常温常压下,18g水的原子数为3NA |
| D、32gO2与O3的混合物含有分子数为NA |
在下列分类中,前者包含后者的是( )
| A、物质的量、摩尔质量 |
| B、置换反应、氧化还原反应 |
| C、化合物、电解质 |
| D、胶体、分散系 |
下列比较中,正确的是( )
| A、原子半径:Na>Mg |
| B、碱性:NaOH>KOH |
| C、结合H+的能力:CO32-<Cl- |
| D、还原性:I-<Br- |
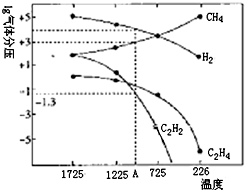 乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.
乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.