题目内容
下列叙述正确( )
| A、标准状况下,1mol任何物质的体积约为22.4L |
| B、1mol气体的体积约为22.4L |
| C、1mol氖气和1mol氧气体积相同 |
| D、标准状况下,1mol 空气的体积约为22.4L |
考点:物质的量的相关计算,气体摩尔体积
专题:计算题,化学用语专题
分析:A.标况下,1mol气体的体积约是22.4L,固体、液态则不一定;
B.物质的量一定时,温度、压强会影响气体的体积;
C.氖气与氧气所处的状态不一定相同;
D.标况下,1mol气体的体积约是22.4L,可以是单一气体,也可以是共存的混合气体.
B.物质的量一定时,温度、压强会影响气体的体积;
C.氖气与氧气所处的状态不一定相同;
D.标况下,1mol气体的体积约是22.4L,可以是单一气体,也可以是共存的混合气体.
解答:
解:A.标况下,1mol气体的体积约是22.4L,固体、液态则不一定,故A错误;
B.物质的量一定时,温度、压强会影响气体的体积,标况下,1mol气体的体积约是22.4L,不是标准状况,1mol气体的体积不一定是22.4L,故B错误;
C.若二者处于相同条件下,则1mol氖气和1mol氧气体积相同,但氖气与氧气所处的状态不一定相同,二者体积不一定相等,故C错误;
D.标况下,气体摩尔体积为22.4L/mol,可以是单一气体,也可以是共存的混合气体,故标准状况下,1mol 空气的体积约为22.4L,故D正确,
故选D.
B.物质的量一定时,温度、压强会影响气体的体积,标况下,1mol气体的体积约是22.4L,不是标准状况,1mol气体的体积不一定是22.4L,故B错误;
C.若二者处于相同条件下,则1mol氖气和1mol氧气体积相同,但氖气与氧气所处的状态不一定相同,二者体积不一定相等,故C错误;
D.标况下,气体摩尔体积为22.4L/mol,可以是单一气体,也可以是共存的混合气体,故标准状况下,1mol 空气的体积约为22.4L,故D正确,
故选D.
点评:本题考查学生对气体摩尔体积的理解,难度不大,注意气体摩尔体积的使用条件及对象,以是单一气体,也可以是可以共存的混合气体.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
目前,科学家正在研究开发一种高能电池--钠硫电池,它以熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na+xS?Na2Sx,下列说法中正确的是( )
| A、放电时Na作正极,S极发生还原反应 |
| B、充电时,钠极与外电源的正极相连 |
| C、充电时阳极反应为:xS2--2e-=xS |
| D、若放电时转移0.2 mol 电子,则用去的钠为4.6g |
下列说法中不正确的是( )
| A、维生素C具有还原性,在人体内起抗氧化作用 |
| B、为防止月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁 |
| C、由水电离出来的c(H+)=1×10-13mol/L的溶液中:K+、CO32-、Cl-、NO3-可能大量共存 |
| D、使石蕊变红的溶液中:Na+、I-、Cl-、NO3-可能大量共存 |
t℃时在一烧杯中盛有一定量KCl溶液,若向该溶液中加x g KCl晶体,充分搅拌后仍有y g晶体未溶:若将原溶液加热蒸发掉zg水,再冷却到t℃,溶液恰好达到饱和.则t℃时KCl的溶解度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
室温下,0.1mol?L-1 HF溶液与0.1mol?L-1 NaOH溶液等体积混合(忽略混合前后溶液体积的变化),则下列有关混合后的溶液中离子浓度的叙述正确的是( )
| A、由水电离产生的c(H+)为1.0×10-7mol?L-1 |
| B、c(F-)+c(HF)=c(Na+) |
| C、升高温度,c(F-)增大 |
| D、c(F-)>c(Na+)>c(H+)>c(OH-) |
下列说法正确的是( )
| A、热化学方程式中的化学计量数只表示物质的量,因此可用分数或小数表示 |
| B、热化学方程式中表明的热量是指每摩尔反应物反应时吸收或放出的热量 |
| C、1 mol碳燃烧所放出的热量为燃烧热 |
| D、1 mol强酸和1 mol强碱完全反应所放出的热量称为中和热 |
 葡萄糖氧化是人体获得能量的途径之一.某同学利用葡萄糖的氧 化反应原理,设计了如图所示的装置.下列说法正确的是( )
葡萄糖氧化是人体获得能量的途径之一.某同学利用葡萄糖的氧 化反应原理,设计了如图所示的装置.下列说法正确的是( )| A、若形成原电池时,B极是负极 |
| B、加入H2SO4,溶液中H+向A极移动 |
| C、加入NaOH,A的电极反应式为C6H12O6-24e-+36OH-═6CO32-+24H2O |
| D、不再添加任何试剂,该装置即能获得电流 |
下列化学用语表达正确的是( )
A、磷原子的原子结构示意: |
B、钠离子的电子式: |
C、甲烷的结构式: |
| D、质子数为8,中子数为10的核素:10O |
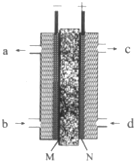 甲醇是燃料电池的常见原料,现已熔融的K2CO3为电解质,以甲醇为燃料,空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.如图是甲醇燃料电池模型,试回答下列问题:
甲醇是燃料电池的常见原料,现已熔融的K2CO3为电解质,以甲醇为燃料,空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.如图是甲醇燃料电池模型,试回答下列问题: