题目内容
20.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 使pH试纸显深蓝色的溶液:Na+、K+、I-、NO${\;}_{3}^{-}$ | |
| B. | 0.1mol•L-1的Ca(ClO)2溶液:K+、Na+、I-、Cl- | |
| C. | 能使甲基橙显红色的溶液:K+、Fe2+、Cl-、NO${\;}_{3}^{-}$ | |
| D. | 加KSCN显红色的溶液:Na+、Mg2+、I-、SO${\;}_{4}^{2-}$ |
分析 A.使pH试纸显深蓝色的溶液,显碱性;
B.离子之间发生氧化还原反应;
C.能使甲基橙显红色的溶液,显酸性;
D.加KSCN显红色的溶液含Fe3+,离子之间发生氧化还原反应.
解答 解:A.使pH试纸显深蓝色的溶液,显碱性,该组离子之间不反应,可大量共存,故A正确;
B.I-、ClO-发生氧化还原反应,不能大量共存,故B错误;
C.能使甲基橙显红色的溶液,显酸性,H+、Fe2+、NO3-发生氧化还原反应,不能共存,故C错误;
D.加KSCN显红色的溶液含Fe3+,Fe3+、I-发生氧化还原反应,不能共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成生石灰;
②在海水中加入生石灰,过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤;
④在氯化氢热气流中加热晶体;
⑤电解上述所得盐(熔融条件下).
下列说法正确的是( )
①把贝壳制成生石灰;
②在海水中加入生石灰,过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤;
④在氯化氢热气流中加热晶体;
⑤电解上述所得盐(熔融条件下).
下列说法正确的是( )
| A. | 向洗涤液中滴加氯化钙溶液可检验沉淀是否洗涤干净 | |
| B. | 上述变化过程中包括了分解、化合、复分解、置换等四种反应类型 | |
| C. | 步骤④在氯化氢热气流中加热晶体的目的是为了防止氯化镁水解 | |
| D. | 步骤⑤也可以采用电解该盐水溶液的方法 |
8.设NA为阿伏加德罗常数的数值.则下列说怯中正确的是
①2.24L氨气含有NA个电子
②1.4g乙烯与丙烯的混合气体含有NA个碳原子
③精炼铜,若阳极失去2NA个电予.则阴极增重64g
④标准状况下,22.4L空气含有NA个分子
⑤过氧化钠与水反应.若电子转移2NA,则产生的氧气为32g
⑥将IL2mol/L的FeCl3溶液加人到沸水中.加热使之完全反应.所得氢氧化铁子数为2NA
⑦在1L0.1mol/L的碳酸钠溶液中.阴离子总数大于0.1NAA.
①2.24L氨气含有NA个电子
②1.4g乙烯与丙烯的混合气体含有NA个碳原子
③精炼铜,若阳极失去2NA个电予.则阴极增重64g
④标准状况下,22.4L空气含有NA个分子
⑤过氧化钠与水反应.若电子转移2NA,则产生的氧气为32g
⑥将IL2mol/L的FeCl3溶液加人到沸水中.加热使之完全反应.所得氢氧化铁子数为2NA
⑦在1L0.1mol/L的碳酸钠溶液中.阴离子总数大于0.1NAA.
| A. | ③④⑤⑦ | B. | ①③④⑦ | C. | ②③④⑤⑦ | D. | ②④⑤⑦ |
15.在15.2g铁和铜的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列X的组成合理的是( )
| A. | 0.3molNO2、0.1molNO | B. | 0.6molNO | ||
| C. | 0.3molNO、0.1molNO2 | D. | 0.2molNO2、0.2molNO |
5.下列判断不合理的是( )
| A. | NH3的水溶液能导电,因此NH3是电解质 | |
| B. | 焰色反应是物理变化 | |
| C. | 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 | |
| D. | 蔗糖、碳酸钡和水分别属于非电解质、强电解质和弱电解质 |
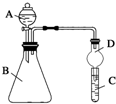 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验. 和
和 F.
F. 和CH2=CH-CH3G.
和CH2=CH-CH3G.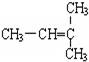 和
和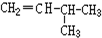
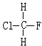 与
与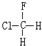 B.
B.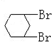 与
与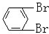 C.
C.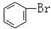 与
与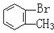 D.
D.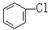 与
与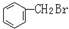 E.ClC(CH3)3与(CH3)2CHCH2Cl F.
E.ClC(CH3)3与(CH3)2CHCH2Cl F.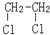 与CH3-CH2Cl.
与CH3-CH2Cl.