题目内容
下列有机化学方程式书写正确的
- A.CH4+Cl2
 CH2Cl2+H2
CH2Cl2+H2 - B.H2C=CH2+Br2→CH3CHBr2
- C.CH3CH2OH+CH3COOH
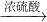 CH3COOCH2CH3
CH3COOCH2CH3 - D.2CH3CH2OH+O2
 2CH3CHO+2H2O
2CH3CHO+2H2O
D
分析:A、氯气和甲烷发生取代反应,有机物分子里的某些原子或原子团被其他的原子或原子团所替代的反应叫取代反应,据此分析;
B、乙烯和溴发生加成反应,有机物分子里的不饱和键两端的碳原子与其他的原子或原子团直接结合生成新的化合物的反应叫加成反应;
C、乙醇和乙酸在浓硫酸的作用下发生酯化反应;
D、乙醇和氧气在铜作催化剂、加热条件下发生氧化还原反应生成乙醛和水.
解答:A、氯气和甲烷发生取代反应,方程式为CH4+Cl2 CH3Cl+HCl,故A错误;
CH3Cl+HCl,故A错误;
B、乙烯和溴发生加成反应,方程式为H2C=CH2+Br2→CH2BrCH2Br,故B错误;
C、乙醇和乙酸在浓硫酸的作用下发生酯化反应,反应方程式为CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O,故C错误;
CH3COOCH2CH3+H2O,故C错误;
D、乙醇和氧气在铜作催化剂、加热条件下发生氧化还原反应生成乙醛和水,反应方程式为2CH3CH2OH+O2 2CH3CHO+2H2O,故D正确.
2CH3CHO+2H2O,故D正确.
故选D.
点评:本题考查了化学反应方程式的书写,难度不大,书写化学反应方程式时要注意化合物的断键方式.
分析:A、氯气和甲烷发生取代反应,有机物分子里的某些原子或原子团被其他的原子或原子团所替代的反应叫取代反应,据此分析;
B、乙烯和溴发生加成反应,有机物分子里的不饱和键两端的碳原子与其他的原子或原子团直接结合生成新的化合物的反应叫加成反应;
C、乙醇和乙酸在浓硫酸的作用下发生酯化反应;
D、乙醇和氧气在铜作催化剂、加热条件下发生氧化还原反应生成乙醛和水.
解答:A、氯气和甲烷发生取代反应,方程式为CH4+Cl2
 CH3Cl+HCl,故A错误;
CH3Cl+HCl,故A错误;B、乙烯和溴发生加成反应,方程式为H2C=CH2+Br2→CH2BrCH2Br,故B错误;
C、乙醇和乙酸在浓硫酸的作用下发生酯化反应,反应方程式为CH3CH2OH+CH3COOH
 CH3COOCH2CH3+H2O,故C错误;
CH3COOCH2CH3+H2O,故C错误;D、乙醇和氧气在铜作催化剂、加热条件下发生氧化还原反应生成乙醛和水,反应方程式为2CH3CH2OH+O2
 2CH3CHO+2H2O,故D正确.
2CH3CHO+2H2O,故D正确.故选D.
点评:本题考查了化学反应方程式的书写,难度不大,书写化学反应方程式时要注意化合物的断键方式.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
硫化钠和碳酸钠为原料、采用下述装置制备硫代硫酸钠,制备反应可表示为:
2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2.根据要求回答问题:
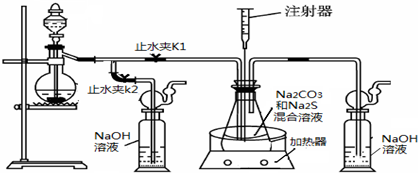
(1)实验时,打开K1,关闭K2,最后洗气瓶中发生反应的离子方程式是______.
(2)锥形瓶内溶液pH小于7时会导致产品分解,因此实验过程中需要控制锥形瓶内溶液的pH.
①反应过程中,锥形瓶中溶液pH将______(填“增大”、“减小”或“保持不变”).
②测量锥形瓶中溶液pH时,用注射器吸取溶液样品比直接打开锥形瓶中瓶塞取样,除操作简便外,还具有的优点是______.
③若实验过程中测得溶液pH已接近于7.此时应该进行的操作是______.
(3)已知:2Na2 S2O3+I2=2NaI+Na2 S4O6.实验结束后进行相关处理,可即获得Na2 S2O3?5H2O晶体.为测量其纯度,取晶体样品mg,加水溶解后,滴入几滴淀粉溶液,用0.010mol/L碘水滴定到终点时,消耗碘水溶液vmL,则该样品纯度是______
(4)制取硫代硫酸钠的另一种方法是直接将硫粉和亚硫酸钠、水混合共热制取.为探究制取硫代硫酸钠最佳条件(溶液pH、亚硫酸钠浓度、反应温度、硫粉质量),设计如下对比实验(每次实验时亚硫酸钠质量均为63g,反应时间为30min):
| 实验序号 | 溶液pH | 亚硫酸钠与水的质量比 | 反应温度 | 硫粉质量 | 亚硫酸钠转化率 |
| 1 | 10 | 1.5:1 | 100 | 18 | 80.7% |
| 2 | a | 1.1:1 | 100 | 18 | 94.6% |
②若还要探究溶液pH、反应温度、硫粉质量对亚硫酸钠转化率的影响,除实验1、2外,至少还需进行______次对比实验.
③实验表明:亚硫酸钠转化率不受硫粉质量多少的影响.为什么?答:______.



 、Cl-
、Cl-