题目内容
4.室温下,有两种溶液:①0.01mol•L-1 NH3•H2O 溶液、②0.01mol•L-1 NH4Cl 溶液,下列操作可以使两种溶液中 c(NH4+)都增大的是( )| A. | 通入少量 HCl 气体 | B. | 加入少量 NaOH 固体 | ||
| C. | 加入少量 H2O | D. | 适当升高温度 |
分析 A.HCl溶于水后的盐酸是强酸,与①NH3•H2O 反应,c(NH4+)增大;盐酸中的氢离子抑制了铵离子的水解,c(NH4+)也增大;
B.氢氧化钠属于强碱,加入少量NaOH固体,溶液中的c(OH-)增大,抑制了氨水的电离;氢氧根离子结合铵离子生成一水合氨,铵离子浓度减小;
C.加入少量H2O,溶液被稀释,两种溶液中c(NH4+)都会减小;
D.升高温度,②氨气会从溶液中挥发出来,导致NH3•H2O 浓度减小,c(NH4+)自然减小;②NH4Cl溶液,升高温度后,促进了水解,c(NH4+)减小.
解答 解:A.HCl溶于水后得到的盐酸是强酸,能够和①NH3•H2O 反应,导致溶液中c(NH4+)增大;盐酸中的H+离子抑制了NH4+的水解,使氯化铵溶液中的c(NH4+)也增大,故A正确;
B.加入少量NaOH固体,溶液中的c(OH-)增大,抑制了NH3•H2O 溶液的电离;氢氧根离子结合NH4+生成一水合氨,c(NH4+)都会减小,所以两溶液中铵离子浓度都减小,故B错误;
C.当向①0.01mol L-1NH3•H2O ②0.01mol L-1NH4Cl加入少量H2O后,溶液被稀释了,两溶液中的c(NH4+)都会减小,故C错误;
D.温度升高,氨气具有挥发性,导致氨气挥发,NH3•H2O 浓度减小,溶液中的c(NH4+)减小;而NH4Cl溶液中,铵根离子的水解为吸热反应,升高温度可以促进NH4+水解,导致c(NH4+)减小,故D错误;
故选A.
点评 本题考查了弱电解质的电离及其影响,题目难度中等,明确电离平衡及其影响为解答关键,注意掌握盐的水解原理,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
14.下列关于节能与可再生能源表述不正确的是( )
| A. | “低碳”意指更低的二氧化碳气体的排放 | |
| B. | 太阳能、水能、风能都属于可再生能源 | |
| C. | 太阳能电池的工作原理是光能与化学能的转换 | |
| D. | 利用燃气轮机进行天然气发电不属于可再生能源利用 |
12.两片铁片分别与足量的盐酸和氯气完全反应,生成的氢气和消耗的氯气体积相同(在相同条件下),则两片铁片的质量比为( )
| A. | 1:1 | B. | 1:3 | C. | 2:3 | D. | 3:2 |
19.如图实验装置和试剂的选用或操作都正确的是( )
| A. | 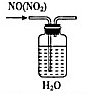 除去NO中的NO2 | B. | 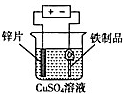 铁制品表面镀锌 | C. | 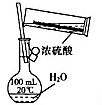 稀释浓硫酸 | D. | 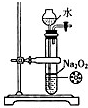 制备少量O2 |
9.下列有机化合物中,既能与盐酸起反应,又能与NaOH溶液反应的是( )
| A. | 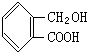 | B. | 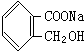 | C. | H2NCH2COONa | D. | H2NCH2COOH |
16.关于如图装置图的叙述中,不正确的是( )
| A. | 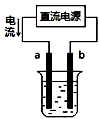 用装置精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 | |
| B. | 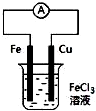 装置的总反应是:Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 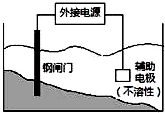 装置中钢闸门应与外接电源的负极相连 | |
| D. | 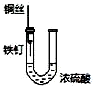 装置中的发生的是铁钉的析氢腐蚀 |
13.关于N2、N2O、N2O5的叙述,正确的是( )
| A. | 每个分子中都含有氮分子 | B. | 每个分子中的氮原子个数相等 | ||
| C. | 每种物质中氮元素的质量分数相同 | D. | 都属于氧化物 |
14.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 饱和氯水中 Cl-、NO3-、Na+、SO32- | |
| B. | pH=12的溶液中 NO3-、I-、Na+ | |
| C. | NaHS溶液中 SO42-、K+、Cl-、Al3+ | |
| D. | 使甲基橙变红的溶液中 C6H5O-、K+、SO42-、Br- |