题目内容
2.某气体可能含有NH3、HCl、CO、H2、CO2中的一种或几种,在恒温恒压下将其通过浓硫酸时,总体积基本不变;再通过足量的澄清石灰水,未见浑浊,但总体积减小;把剩余气体导出后点燃,燃烧产物不能使无水硫酸铜变蓝.则原气体中一定有( )| A. | CO和HCl | B. | H2,HCl和CO | C. | CO2,CO和HCl | D. | CO2,CO |
分析 某气体可能含有NH3、HCl、CO、H2、CO2中的一种或几种,在恒温恒压下将其通过浓硫酸时,总体积基本不变,可知混合气体中不含NH3;根据通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,说明有气体被吸收;在O2中能够点燃,燃烧产物不能使CuSO4粉末变色说明没有水蒸气生成进行解答.
解答 解:某气体可能含有NH3、HCl、CO、H2、CO2中的一种或几种,在恒温恒压下将其通过浓硫酸时,总体积基本不变,可知混合气体中不含NH3;通过过量的澄清石灰水,未见变浑浊,一定不含二氧化碳气体,但混合气体的总体积减小,说明有气体被吸收,只能是HCl气体,说明含有HCl;在O2中能够点燃,燃烧产物不能使CuSO4粉末变色说明没有氢气,故原混合气体中含有HCl和CO,没有氢气和二氧化碳气体,故选A.
点评 本题考查混合气体的组成判断,难度不大,做题时注意从物质反应的典型现象入手判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.已知四种白色粉末分别是硝酸钾、氯化镁、氢氧化钡、无水硫酸铜中的一种.现只提供蒸馏水一种试剂,对这些物质进行鉴别(被鉴别出的物质可作为试剂来鉴别其他物质).请按要求填写下列表格:(注意:用化学式填写)
(1)步骤1:
(2)步骤2:
(3)步骤3:
(1)步骤1:
| 加入试剂 | 被检出物质 | 理由 |
| 水 | CuSO4 | CuSO4溶于水溶液显蓝色 |
| 加入试剂 | 被检出物质 | 离子方程式 |
| CuSO4 |
| 加入试剂 | 被检出物质 | 离子方程式 |
| MgCl2 |
14.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 2g氢气所含原子数目为NA | |
| B. | 标准状况下,11.2L H2O所含分子数为0.5NA | |
| C. | 1mol•L-1 CaCl2溶液中所含Ca2+离子的数目为NA | |
| D. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
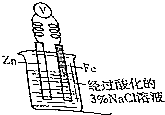 钢铁是用量最大、用途最广的合金,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.
钢铁是用量最大、用途最广的合金,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.